Образование - бутен
Cтраница 2
Эти сведения были использованы для доказательства того, что пути образования бутенов-2, вероятно, одинаковы и что бутен-1 образуется по более сложному механизму. Распределение дейтерия в олефинах, в условиях, когда они свободно изомеризу-ются, очень сходны, однако маловероятно, что образование бутена - 1 идет через изомеризацию ц с-бутена-2. Более того, если изомеризация цнс-бутена-2 происходит перед его десорбцией, то, как следует из данных о его изомеризации ( см. раздел II), образование гранс-бутена-2 и бутена-1 в соотношениях, указанных в табл. 31, маловероятно. [16]
Однако при 130 С наблюдается бурная реакция; при этом получаются хлористый водород, бутен. Реакция между пятихлористым фосфором ( 3 моль) и три-к-бутилборатом ( 2 моль) при 70 С протекает медленно ( в течение 4 ч) с образованием бутена, хлористого водорода, к-бутилхлорида и хлорокиси фосфора. При избытке бората ( 5 моль бората на 3 моль РС1а) в реакцию вступает и хлор-окись фосфора, но при достаточно высокой температуре. Входящий в ее состав сильно электрофильный ион [ РС14 ] конкурирует с бором за свободную пару электронов кислорода. [17]
Гриньяра катализирует гидрирование бутадиена до бутана. Однако при использовании Cp2VCl2 реакция останавливается на стадии образования бутена. [18]
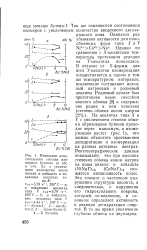 |
Изменение относительного состава изомерных бутенов ( в абс. и отн. % с увеличением количества ионов никеля и кобальта в никелевых цеолитах типа X. [19] |
В отличие от Х - формы для всех У-цеолитов изомеризация осуществляется в одном и том же температурном интервале, исключение составляют исходный натриевый и родиевый цеолиты. На цеолитах типа X и У с увеличением степени обмена образование бутенов проходит через максимум, а изомеризация растет ( рис. 1), что можно объяснить протеканием дегидратации и изомеризации на разных активных центрах. Рентгенографические данные показывают, что при высоких степенях обмена ионов натрия на ионы никеля и кобальта ( № ЫаУ) 12, ( СоКаУ) 12 снижается интенсивность полос. Это говорит о частичном разрушении структуры цеолита, а следовательно, о нарушении его гидроксильного покрова, который, по-видимому, в основном определяет активность в реакции дегидратации спиртов. [20]
Время циклов при этом варьировалось в интервале 2 - 30 с, а величина амплитуды колебаний - от 0 2 до 1 ( рис. 2.1) г Производительность т ] по бутену, как видно на рис. 2.1, увеличивается с уменьшением длительности цикла, а избирательность s, наоборот, увеличивается с увеличением продолжительности колебаний. Это объясняется таким предполагаемым механизмом реакции гидрирования, по которому скорость образования побочного продукта - бутана - сильно зависит от концентрации водорода. С уменьшением величины периода колебаний количество адсорбированного бутадиена увеличивается, что приводит к увеличению скорости образования бутена и к еще большему ( относительному) увеличению скорости образования бутана. При медленных переключениях среднее количество адсорбированного бутадиена уменьшается, обеспечивая увеличение избирательности процесса. [22]
Из опытных данных следует, что наибольшей селективностью в соди-меризации этилена и пропилена обладает катализатор NiCb / NaX. Тот факт, что катализатор NiCb / NaX селективнее в содимеризации катализатора NiC / Al-Si указывает на то, что цеолит NaX, не обладающий протонной кислотностью, является важной частью нанесенного гетерогенного катализатора координационного типа. По мере увеличения количества циклов реакция-регенерация на катализаторе NiCl2 / NaX конверсия уменьшается, а селективность образования бутенов и пентенов возрастает. [23]
 |
Равновесие изомеризации бутенов с прямой цепочкой в 2-метил - 1-пропен. [24] |
Расчет по таблицам Ф - потенциалов, приведенным во втором выпуске Справочника ( табл. 30), не дает совпадения с экспериментом. Расхождения с экспериментом достигают 100 % в значении константы равновесия. Причиной этого, как удалось показать одному из нас [3], является неточность, допущенная в определении теплоты изомеризации н-бутана в изобутан, которая лежит в основе вычисления теплот образования бутенов. [25]
Например, они заметно различаются в присутствии платинового или палладие-вого катализаторов. Соотношение между скоростями, установленное для чистых углеводородов, не сохраняется при гидрировании их смесей. Поэтому, несмотря на то, что скорости гидрирования чистого бутадиена в бутен и чистого бутена в бутан практически являются теми же, в смеси этих соединений гидрирование бутадиена ( с образованием бутена) протекает намного быстрее. Возможно, это объясняется большей величиной коэффициента хемосорбции бутадиена. [26]
Например, они заметно различаются в присутствии платинового или палладие-вого катализаторов. Соотношение между скоростями, установленное для чистых углеводородов, не сохраняется при гидрировании их смесей. Поэтому, несмотря на то, что скорости гидрирования чистого бутадиена в бутен и чистого бутена в бутан практически являются теми же, в смеси этих соединений гидрирование бутадиена ( с образованием бутена) протекает намного быстрее. Возможно, это объясняется большей величиной коэффициента хемосорбцин бутадиена. [27]
Страницы: 1 2
