Образование - псевдоколлоид
Cтраница 2
Вопрос о состоянии щелочных металлов в случае микроконцентраций может рассматриваться лишь в связи с их адсорбционными свойствами и образованием псевдоколлоидов. [16]
При еще меньших концентрациях продукты гидролиза проявляют сильную склонность к адсорбции на стенках сосуда или присутствующих в растворе посторонних коллоидных частицах с образованием псевдоколлоидов. [17]
 |
Сорбция цезия стеклом. [18] |
Вместе с тем слабая адсорбция цезия кварцевым стеклом ( что находится в согласии с данными, полученными для натрия [312]) указывает на малую вероятность образования псевдоколлоидов щелочных металлов в ощутимых количествах; иначе говоря, регистрация псевдоколлоидов в растворе возможна только при достаточно большой емкости кремнекислых загрязнений. [19]
Как видно из рис. 58, процент коллоидной формы увеличивается симбатно с ростом адсорбции Рт147 на кварцевом стекле. Такое поведение характерно для образования псевдоколлоидов. [20]
 |
Диализ растворов La140.| Ультрафильтрация Рт147 через целлофан. [21] |
Как видно из рис. 120, процент коллоидной формы увеличивается симбатно с ростом адсорбции Рт147 на кварцевом стекле. Такое поведение характерно для образования псевдоколлоидов. [22]
 |
Центрифугирование Са45 из кальция, бесконечно разбавленных растворов. Центрифугирование растворов кальция показало. [23] |
Образование истинных коллоидов Са ( ОН) 2 в случае микроконцентраций радиоактивного изотопа невозможно. Было проведено исследование I133 ] адсорбционных свойств кальция для выяснения возможности образования псевдоколлоидов. [24]
Однако нельзя произвольно переносить свойства Na и Cs на все радиоактивные изотопы. Адсорбционная способность элемента зависит от целого ряда переменных, в том числе от заряда и радиуса иона. Поэтому наблюдающаяся у различных элементов тенденция к образованию псевдоколлоидов требует в каждом отдельном случае специального изучения. [25]
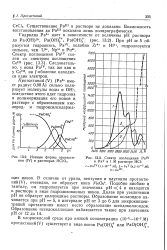 |
Ионные формы протактиния ( IV в растворах НС1О4.| Спектр поглощения Pa V и PaV в 1 М растворе НС1. [26] |
Подобно ниобию и танталу, он гидролизуется при значениях рН 4 и находится в растворе в виде гидролизованных ионов. Далее при увеличении рН он образует коллоидные растворы. Образование коллоидов начинается при рН 5, в интервале рН от 3 до 6 для микроконцентраций протактиния имеет место образование псевдоколлоидов. [27]
В нейтральных и слабощелочных средах америций проявляет коллоидные свойства. Вместе с тем определить природу коллоидов и попытаться разграничить области существования америция в псевдоколлоидном и истинноколлоидном состоянии можно, лишь применив дополнительные методы исследования, определяющие заряд и дисперсность частиц. В частности, из данных по центрифугированию и электромиграции следует [272 273], что коллоидное поведение америция при рН 6 - 8 связано с образованием псевдоколлоидов. В равновесии с грубодисперсной фазой псевдоколлоидов существуют положительно заряженные гидро-лизованные ионы америция, что подтверждается наличием максимума на адсорбционной кривой. [28]
С повышением рН раствора от 2 до 5 наблюдается резкое повышение сорбционной способности протактиния. Данные по электрофорезу указывают на то, что в этой области рН преобладающей формой нахождения протактиния в растворе является также положительно заряженные частицы. Следовательно, с понижением заряда катионов протактиния сорбционная способность их резко повышается. Можно предполагать, что это происходит вследствие дегидратации ионов по мере понижения заряда их, что значительно облегчает подход ионов к поверхности сорбента. Помимо того, очевидно, некоторую роль играет понижение конкуренции со стороны ионов водорода, а также повышение отрицательного заряда стекла с увеличением рН раствора. Повышение сорбционной способности ионов протактиния вызывает резкий подъем в процессе образования псевдоколлоидов. Наблюдается выраженный подъем на кривой ультрафильтрации; ультрафильтр, очевидно, задерживает крупные частицы загрязнений с сорбированным на них протактинием. [29]
Использование очень разб р-ров радиоактивных элементов в большой мере расширяет область применимости радиохимич. При распределении микроколичеств изотопов между фазами макросостав фаз практически не меняется, именно поэтому радиохимич. Сюда же относятся и законы распределения радиоактивных веществ между двумя жидкими или между газовой и конденсированными фазами. Экспериментальные исследования с микроколичествами вещества имеют свою специфику. Исключительно важное значение приобретают процессы адсорбции микрокомпонента на примесях с образованием псевдоколлоидов, изменение окислительно-восстановительных потенциалов, присутствие изотопных примесей и пр. [30]
Страницы: 1 2 3