Образование - двойная тройная связь
Cтраница 1
Образование двойных и тройных связей побуждается, по-видимому, устойчивостью внешнего октета. Например, владея тремя общими парами электронов, ядра азота в молекуле азота действительно приобретают октеты электронов. [1]
На образование двойной и тройной связи тратится энергии больше, чем на образование простой, но меньше, чем на образование двух или трех простых связей. [2]
При образовании двойных и тройных связей ( кратных) наблюдается большее выделение энергии, чем в случае образования простых связей. Атомы углерода, связанные кратной связью, располагаются ближе друг к другу. В образовании этих связей принимают участие электроны, слабо связанные в молекуле. Поэтому по месту двойной связи молекула способна присоединять другие атомы, проявляя ненасыщенность. [3]
 |
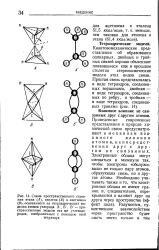
Пространетпенная модель л-связи в этилене, [ IMAGE ] Схема or - связс-й бензола. сг - -... -. [4] |
Иначе происходит образование двойных и тройных связей в ненасыщенных соединениях. Остающиеся у углеродных атомов негибридизированные р-электроны, орбитали которых располагаются перпендикулярно плоскости а-связей, перекрываются друг с другом, образуя я-связь. Так как перекрывание орбиталей здесь не такое глубокое, то я-связь значительно лабильнее и легче поляризуется и разрывается, чем сг-связь. [5]
Иначе происходит образование двойных и тройных связей в ненасыщенных соединениях. Остающиеся у углеродных атомов негибридизированные р-электроны, орбитали которых располагаются перпендикулярно плоскости а-связей, перекрываются друг с другом, образуя я-связь. Так как перекрывание орбиталей здесь не такое глубокое, то я-связь значительно лабильнее и легче поляризуется и разрывается, чем а-связь. [6]
Иначе происходит образование двойных и тройных связей в ненасыщенных соединениях. В этилене, например, каждый углеродный атом образует связи с тремя партнерами, на что расходуются электроны s - атомной и двух р-атомных орбит. [7]
Квантовомеханические представления об образовании одинарных, двойных и тройных связей хорошо объясняют появившиеся еще в прошлом столетии стереохимические модели этих видов связи. [9]
Квантовомеханические представления об образовании ординарных, двойных и тройных связей хорошо объясняют появившиеся еще в прошлом столетии стереохимические тетраэдрические модели этих видов связи. [10]
Кроме того, кремний не способен к образованию двойных и тройных связей. Это касается не только кратных связей между атомами кремния, но и между атомом кремния и другими элементами. [11]
Причина изменения этого порядка заключается, конечно, в том, что молекулы алкенов и алкинов упрочены образованием двойных и тройных связей. Это и обусловило резкое падение от СН2 к С2Н4 и от С к С2Н2 при последующем уже некрутом ходе-гомологических линий алкенов и алканов на рис. 126; на линии алканов резкого падения от СН4 к С2Не нет, так как отсутствует и причина - образование кратной связи. Данный пример подчеркивает важность того, что положение энергетического уровня молекулы зависит от ее структуры и природы ее связей. [12]
Одинарные связи образуются при обобществлении двух электронов ( часто по одному от каждого из атомов), а образование двойной и тройной связи связано с обобществлением соответственно четырех или шести электронов. [13]
Атом 81 имеет большую величину атомного радиуса ( 0 133 нм) в сравнении с атомным радиусом С ( 0 077 нм); для него не характерно образование двойных и тройных связей. [14]
Углерод легко образует длинные углеродные цепи с большим числом атомов углерода; кремний с трудом образует небольшие цепочки. Кроме того, кремний не способен к образованию двойных и тройных связей. Это касается не только кратных связей между атомами кремния, но и между атомом кремния и другими элементами. [15]
Страницы: 1 2