Образование - недиссоциированное соединение
Cтраница 2
На рисунке 5 изображена диаграмма вязкости системы вода - бромаль с образованием диссоциированного соединения. На рис. 6 изображены диаграммы вязкости и плотности системы алли-ловое горчичное масло - ме-тиланилин с образованием недиссоциированного соединения аллил-метил-фенил-тио - мочевины. [16]
 |
Особые точки кривых. а - узловая. б - угловая. в - изолированная. г - возврата. д - уединенная точка превращения. [17] |
Пунктирными кривыми показаны действительные касательные, которые можно провести к особым точкам. К изолированной точке может быть проведена только мнимая касательная. Курнакова состояла в том, что экстремумы на диаграммах свойств при образовании недиссоциированных соединений принимались за особые ( сингулярные) точки. [18]
Сопоставление результатов, полученных всеми авторами, работавшими над данной системой, позволяет нам сделать некоторые выводы по поводу особенностей изученной равновесной диаграммы. Ледя: кое поле изученной системы носит сингулярный характер; изотермы ледяного поля образуют сингулярную антиклинальную складку. Сопоставляя ледяное поле системы Na2C l2 - PtCl4 - Н2О с ледяным полем системы FeCl3 - - HC1 - Н2О ( рис. 3), мы видим, что в последнем случае изотермы ледяного поля близки к прямым линиям; в этой системе не имеется ни образования недиссоциированных соединений, ни образования устойчивых комплексных солей. [19]
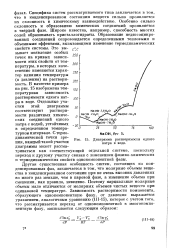 |
Диаграмма растворимости едкого натра в воде. [20] |
Специфика систем рассматриваемого типа заключается в том, что в конденсированном состоянии веществ сильно проявляется их склонность к химическому взаимодействию. Особенно сильно склонность к образованию химических соединений проявляется в твердой фазе. Широко известна, например, способность многих солей образовывать кристаллогидраты. Образование недиссоциированных соединений сопровождается определенными тепловыми и объемными эффектами, вызывающими изменение термодинамических свойств системы. Это вы - с зывает появление особых точек на кривых зависимости этих свойств от температуры, в которых качественно изменяется характер влияния температуры ( и давления) на растворимость. В качестве примера на рис. 15 изображена температурная зависимость растворимости едкого натра в воде. [21]
Рассматриваемый случай интересен двойственностью точки D. При Км 0 точка D теряет свойство особой точки, оставаясь в реальных системах только экстремальной. Он писал поэтому, что сингулярная точка диаграммы в геометрическом понимании этого термина есть признак диссоциации соединения в системе; сингулярная точка исчезает при образовании недиссоциированного соединения. Последнее справедливо только к нестехиометрической особой точке S, получившей название степановской. Она действительно появляется на изотермах выхода только тогда, когда химическое соединение в какой-то степени диссоциировано. Если же степень диссоциации соединения уменьшается и в пределе становится равной нулю, степановская точка на диаграмме выхода исчезает. Стехиометрическая особая точка D существует при отсутствии диссоциации соединения и исчезает на диаграммах реальных систем, в которых соединение АВ2 бывает диссоциировано в какой-то степени. [22]
Страницы: 1 2