Образование - сульфат - свинец
Cтраница 3
В состав пасты до реакции входят сульфат свинца PbSO4, диоксида свинца РЬО2, оксид свинца РЬО и небольшие количества металлического свинца РЬ. Оксиды свинца реагируют с серной кислотой, содержащейся в электролите, с образованием сульфата свинца и воды. Кроме того, в присутствии серной кислоты двуокись свинца и металлический свинец взаимодействуют с образованием сульфата свинца и воды. Использование электролита на стадии сульфатирования позволяет решить проблему удаления отработанного электролита. [31]
Это уравнение работы свинцового аккумулятора было предложено Гледстоном и Трайбом в 1883 г. В то время, однако, механизм электродных процессов аккумулятора еще не был вполне понятен. Теория, выраженная этим уравнением, известна под названием теории двойной сульфитации, тай как она предполагает образование сульфата свинца на обоих электродах; время от времени предлагали и другие теории действия свинцового аккумулятора. Если не считать процессов, которые протекают лишь в незначительной степени, например образование более высоких степеней окисления, чем РЬО2, нет сомнения в том, что реакции, изображенные здесь, представляют основные процессы, протекающие на электродах свинцового аккумулятора. [32]
Аккумуляторы составляют из сшшцовых пластин с нанесенным на них оксидом свинца РЬО. Пластины погружают в раствор серной кислоты. Сначала происходит реакция образования сульфата свинца. [33]
При чтении слева направо это уравнение представляет процесс разряда, справа налево - заряда. Доводы в пользу этой теории, проверявшейся многочисленными исследователями, разнообразны. Одним из таких доказательств является образование сульфата свинца в конце разряда на обеих пластинах. Другим доказательством служит изменение концентрации серной кислоты в процессе заряда и разряда аккумулятора. Важным доводом является состав активных материалов пластин, находящийся в соответствии с уравнением. Активный материал отрицательной пластины - губчатый свинец, его образование при заряде совершенно бесспорно. [34]
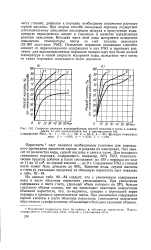 |
Скорость реакции взаимодействия серной кислоты и глета в зависимости от его окисленности ( а и дисперсности ( б. [35] |
Из данных табл. 82 - 84 следует, что с увеличением содержания воды в пасте объемная пористость увеличивается. При увеличении содержания в пасте глета, удельный объем которого на 28 % больше удельного объема свинца, все же происходит некоторое возрастание объемной пористости, что, по-видимому, связано с агрегацией зерен порошка в процессе приготовления пасты. При увеличении содержания серной кислоты в пасте объемная пористость уменьшается вследствие образования сульфата свинца, обладающего большим удельным объемом. [36]
В состав пасты до реакции входят сульфат свинца PbSO4, диоксида свинца РЬО2, оксид свинца РЬО и небольшие количества металлического свинца РЬ. Оксиды свинца реагируют с серной кислотой, содержащейся в электролите, с образованием сульфата свинца и воды. Кроме того, в присутствии серной кислоты двуокись свинца и металлический свинец взаимодействуют с образованием сульфата свинца и воды. Использование электролита на стадии сульфатирования позволяет решить проблему удаления отработанного электролита. [37]
 |
Разрядные характеристики аккумуляторов типа СК. [38] |
Концентрация электролита в порах активной массы в процессе разряда снижается. Это приводит к снижению напряжения на зажимах аккумулятора. Это объясняется тем, что при разрядах большим током в течение малого времени диффузия серной кислоты в поры активной массы не успевает за процессом образования сульфата свинца. Сульфат свинца закрывает доступ к активной массе. Для аккумуляторов СК и СН предельное напряжение при разряде током 3 - 10-часового режима составляет 1 8 В, а при разрядах большим током - 1 75 В. [39]
IX, § 11) основано на окислительных свойствах соединений четырехвалентного свинца и на их переходе в устойчивые соединения двухвалентного свинца. Аккумуляторы составлены из свинцовых пластин с нанесенной на них окисью свинца. Пластины погружают в раствор серной кислоты. Сначала происходит реакция образования сульфата свинца. [40]
 |
Разрядные характеристики аккумуляторов типа СК. [41] |
При разряде реакция читается слева направо. Концентрация электролита в порах активной массы в процессе разряда снижается. Это приводит к снижению напряжения на зажимах аккумулятора. Это объясняется тем, что при разрядах большим током в течение малого времени диффузия серной кислоты в поры активной массы не успевает за процессом образования сульфата свинца. Сульфат свинца закрывает доступ к активной массе. [42]
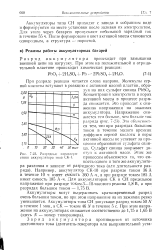 |
Разрядные характеристики аккумулятора типа СК-1. [43] |
При разряде реакция читается слева направо. Концентрация электролита в порах активной массы в процессе разряда снижается. Это приводит к снижению напряжения на зажимах аккумулятора. Напряжение снижается тем больше, чем больше ток разряда ( рнс. Это объясняется тем, что при разрядах большим током в течение малого времени диффузия серной кислоты в поры активной массы не успевает за процессом образования сульфата свинца. Сульфат свинца закрывает доступ к активной массе. [44]
Страницы: 1 2 3