Образование - твердый
Cтраница 1
Образование твердого р-ра на основе ферромагнитного металла приводит к нек-рому возрастанию его коэрцитивной силы ( увеличению магнитной твердости С. Введение второго компонента сверх предела растворимости при комнатной темп-ре и связанное с этим выпадение новой фазы при остывании в значительно большей мере повышает коэрцитивную силу С. [1]
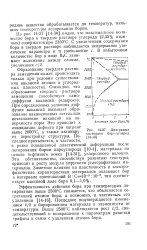 |
Диаграмма состояния бор-углерод. [2] |
Образование твердого раство-ра замещения может происходить только при условии существования вакансий атомов в углеродных плоскостях. При определенных условиях диффузия вакансий вызывает образование вакансионных петель или исчезновение вакансий на поверхности поры. Это приводит к ликвидации дефекта при нагреве выше 2000 С, а также активирует перестройку структуры. Последнее проявляется, в частности, в резко повышенной пластической деформации после легирования бором пироуглерода [10-4], материала на основе нефтяного кокса [14-31], углеродного волокна. Это обстоятельство, способствуя развитию текстуры, приводит к росту модуля упругости углеграфитовых материалов. [3]
Теплота образования твердого ( NH4) 2CO3 составляет 205 3 ккал / моль. [4]
Теплота образования твердого NH4C1 из элементов составляет 75 ккал / г-мол. [5]
Теплота образования твердого 1СЬ и:) элементов равна 21 ккал / моль. В расплавленном состоянии иодтрихлорид ( подобно IC1) обладает довольно хорошей электропроводностью. В парах имеет место равновесие 1С1з 1С1 СЬ, почти нацело смещенное вправо. Растворы 1С13 в крепкой соляной кислоте характеризуются смещенным вправо равновесием по схеме: HCl lCls li НТГ. Пни используются при органических синтезах и анализах сульфидных минералов. [6]
Теплота образования твердого BF3 NH3 из газов при 0, определенная калориметрически, составляет 41 3 ккал. Аммиакат может быть очищен сублимацией [79], он не растворяется в бензоле, сероуглероде, четы-реххлористом углероде, этиловом эфире и в других неполярных или слабополярных растворителях [64, 65], но слабо растворим в спиртах. Это показывает, что BF3 NH3 сам имеет значительный диполъный момент. [7]
Теплота образования твердого BF3 - NH3 из газов при 0, определенная калориметрически, составляет 41 3 ккал. Аммиакат может быть очищен сублимацией [79], он не растворяется в бензоле, сероуглероде, четыреххло-ристом углероде, этиловом эфире и в других неполярных или слабополярных растворителях [64, 65], но слабо растворим в спиртах. Это показывает, чтоВР3 - МН3 сам имеет значительный дипольный момент. [8]
Энтальпия образования твердого [ BN ] из простых тел равна - 60, а для газообразного ( BN) она составляет 148 ккал / моль. Таким образом, энергия конденсации в этом случае громадна, а именно 208 ккал. Именно эта энергия и стабилизует боразон, переводя его в разряд экзотермически образующихся, термически устойчивых, тугоплавких и весьма твердых веществ. [9]
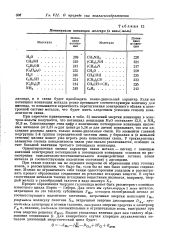 |
Потенциалы ионизации молекул ( в ккал / моль. [10] |
Процесс образования твердого галогенида может быть рассмотрен с помощью известного цикла Борна - Габера. [11]
 |
Потенциалы ионизации молекул ( в ккал / моль. [12] |
Процесс образования твердого галогенида может быть рассмотрен с помощью известного цикла Ворпа - Габера. [13]
Теплота образования твердого ШС14 из элементов, вычисленная по правилу Капустинского [72], составляет - 320 ккал / моль, по данным [1] - 255 ккал / моль, по данным [73], находится в пределах от - 235 до - 293 ккал / моль. [14]
Теплота образования твердого сульфата аммония из газообразного аммиака и серной кислоты составляет 65 44 ккал / моль, теплота образования из элементов равна 281 9 ккал / моль. [15]
Страницы: 1 2 3 4