Образование - фтористый водород
Cтраница 3
Выделенный на аноде, он тотчас взаимодействует с воУ дои с образованием фтористого водорода, кислорода, а также таких побочных продуктов реакции, как озон и пероксид водо - рода. [31]
Зерченинов [80] пересчитал данные Руффа, используя более правильное значение стандартной энтальпии образования фтористого водорода. После уточнения величина ДЯ, 298 становится равной - 28 1 1 9 ккал / моль. [32]
Траубе и Ланге нашли, что при взаимодействии плавикового шпата и серной кислоты в качестве промежуточного продукта образуется фторсульфоновая кислота. В эквимолярных смесях плавикового шпата и H2S04 часть фторида немедленно разлагается с образованием фтористого водорода, который затем может реагировать с частью серной кислоты, не прореагировавшей с плавиковым шпатом, с образованием HSOsF. В результате, реакция между плавиковым шпатом и серной кислотой, вероятно, замедляется. [33]
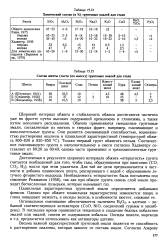 |
Химический состав ( в % грунтовых эмалей для стали.| Состав шихты ( части ( по массе грунтовых эмалей для стали. [34] |
Достигаемая в результате широкого интервала обжига открытость грунта считается необходимой для того, чтобы газы, образующиеся при вжигании ( СО, СОа, Н2), могли при этом удаляться. Для той же цели предназначается в частности и добавка плавикового шпата, реагирующего с водой с образованием летучего фтористого водорода. Необходимость открытости была поставлена под сомнение Рикманом ( 1958), так как при обжиге грунта сквозь слой эмали проходят бесчисленные пузырьки, которые вымывают газ. [35]
Нерастворим в воде, спирте, органических растворителях; в разбавленных кислотах и щелочных соединениях растворим с образованием фтористого водорода. Вещество стойкое, практически не разлагается под действием влаги и света. Получают при сплавлении фосфора с цинком с последующим размолом. Является высокотоксичным ядовитым веществом. [36]
Хладоны химически инертны, не горят, в смеси с воздухом не воспламеняются и не взрываются, термически стабильны. При температуре свыше 400 С ( при соприкосновении с горячими поверхностями или под действием пламени) разлагаются с образованием хлористого и фтористого водорода со следами ядовитого газа - фосгена. [37]
Сродство к водороду у фтора так велико, что фтор отнимает его даже у воды. Так, если па поверхность нагретой воды направить струю фтора, то вода загорается и горит бледно-фиолетовым пламенем с образованием фтористого водорода и кислорода. [38]
Основным преимуществом фреона-12 является относительная безвредность, так как только при содержании его в воздухе более 30 % по объему появляются признаки отравления организма из-за недостатка кислорода. При температурах свыше 400 ( при соприкосновении с горячими поверхностями или действии открытого пламени) происходит разложение фреона с образованием хлористого и фтористого водорода и небольшого количества ( следов) ядовитого газа - фосгена. Пары фреона не оказывают действия на вкус и цвет мясных и молочных продуктов и овощей. [39]
Преимущество фреона-12 - относительная безвредность, так как только при содержании его в воздухе более 30 % по объему появляются признаки отравления организма из-за недостатка кислорода. При температурах свыше 400 С ( при соприкосновении с горячими поверхностями или под действием открытого пламени) фреон разлагается с образованием хлористого и фтористого водорода и небольшого количества ( следов) ядовитого газа-фосгена. Поэтому в машинных отделениях фреоновых установок запрещается курить и размещать электронагревательные приборы. Пары фреона не оказывают действия на вкус и цвет пищевых продуктов. [40]
Избыток олеума свыше 200 % почти не повышает выход BF8; 50 % - ный избыток борного ангидрида при 180 и 200 % - ном избытке олеума понижает выход BF3c82 до 75 6 %, вероятно, в результате образования BFS - B2O3 в жидкой фазе. Для проведения реакции некоторые исследователи [26] рекомендуют, как и в процессе с CaF2, вначале растворять борный ангидрид в серной кислоте, а затем постепенно вводить калиевую соль фторборной кислоты, чтобы воспрепятствовать образованию фтористого водорода. Предлагают также проводить разложение горячей серной кислотой [27] с целью уменьшения ее количества. [41]
Избыток олеума свыше 200 % почти не повышает выход BF3; 50 % - ный избыток борного ангидрида при 180 и 200 % - ном избытке олеума понижает выход BF3 с 82 до 75 6 %, вероятно, в результате образования BF3 В203 в жидкой фазе. Для проведения реакции некоторые исследователи [26] рекомендуют, как и в процессе с CaF2, вначале растворять борный ангидрид в серной кислоте, а затем постепенно вводить калиевую соль фторборной кислоты, чтобы воспрепятствовать образованию фтористого водорода. Предлагают также проводить разложение горячей серной кислотой [27] с целью уменьшения ее количества. [42]
В настоящее время производство простого суперфосфата, который еще недавно был основным фосфорным удобрением, более не развивается. Это обусловлено тем, что в простом суперфосфате невелико содержание питательного вещества, производственный процесс невозможно сколько-нибудь значительно интенсифицировать; кроме того, он сопровождается вредными выбросами в атмосферу, связанными, главным образом, с образованием фтористого водорода. Взамен простого суперфосфата организуется производство концентрированного фосфорного удобрения - продукта взаимодействия фосфорной кислоты с апатитом, так называемого двойного суперфосфату, и сложных удобрений. [43]
Лазерный луч, испускаемый химическим лазером, можно использовать, как и любой другой. Но химический лазер интересен еще и тем, что благодаря обратному действию возникающего излучения на протекающую химическую реакцию можно получить важные данные о механизме и параметрах реакции. Например, для реакции образования фтористого водорода в приведенной выше лазерной системе получены данные о распределении энергии, выделяющейся в результате реакции, по уровням. Установлено, что до 57 % энергии приходится на колебательное движение, до 6 % - на вращательное и до 37 % составляет энергия переноса. [44]
Тионилфторпд и тионплхлоридфторид представляют собой бесцветные газы, которые имеют неприятный запах. По химической реакционной способности тионилхлоридфторид является промежуточным соединением между тионилфторидом и тионилхлоридом. Тионилфторид медленно реагирует с водой с образованием фтористого водорода и сернистой кислоты и инертен к ртути, в то время как смешанный тионилхлоридфторид подвержен быстрому гидролизу и легко реагирует со ртутью. Тионилхлоридфторид неустойчив и медленно диспропорционирует на тионилхлорид и тионилфторид при комнатной температуре. [45]
Страницы: 1 2 3 4