Образование - йодистый водород
Cтраница 3
По мере течения реакции скорость прямой реакции вследствие уменьшения концентраций водорода и иода уменьшается; вместе с тем в результате образования йодистого водорода постепенно увеличивается его парциальное давление и возрастает скорость обратной реакции. В конце концов скорости прямой и обратной реакций сравняются и наступит состояние химического равновесия. [31]
 |
Дипольные моменты галогеноводородов. [32] |
Иод начинает реагировать с водородом также около 225 С; реакция протекает быстро выше 450 С, хотя при этой температуре образование йодистого водорода идет не до конца из-за частичной диссоциации. [33]
Для уменьшения тока фона, образующегося в результате реакции иода с водой ( ШО I2 HI HOI), а также из-за примесей в электролите, которые реагируют с иодом до образования йодистого водорода, в электролитическую ячейку введена вторая пара электродов4, аналогичная измерительной паре, замкнутая накоротко. Эта пара электродов обеспечивает очистку электролита в камере с запасным электролитом перед его поступлением в измерительную камеру и тем самым способствует значительному уменьшению тока фона. [34]
Для уменьшения тока фона, образующегося в результате реакции иода с водой ( Н2О I2 HI HOI), а также из-за примесей в электролите, которые реагируют с иодом до образования йодистого водорода, в электролитическую ячейку введена вторая пара электродов4, аналогичная измерительной паре, замкнутая накоротко. Эта пара электродов обеспечивает очистку электролита в камере с запасным электролитом перед его поступлением в измерительную камеру и тем самым способствует значительному уменьшению тока фона. [35]
Символ: I, формула ( в газообразном агрегатном состоянии): 12; сине-черные пластинчатые кристаллы с металлическим блеском; при нагревании образует фиолетовые едкие пары, при охлаждении которых получают твердый иод; ядовит; слабо растворим в воде: йодная вода ( желтая окраска); растворим в спирте: настойка иода ( коричневая окраска); реагирует с водородом с образованием йодистого водорода. [36]
Выбор между этими механизмами был сделан с помощью фотохимической генерации атомов иода в смеси иода и водорода при достаточно низких температурах, что позволяет пренебречь скоростью термической реакции. Из скорости образования йодистого водорода можно найти величину к70 - Отношение констант скоростей Кбэ / К-69 представляет собой известную константу равновесия диссоциации молекулярного иода на атомы при данной температуре. [37]
Лемуан изучал реакцию образования йодистого водорода из паров иода и водорода и установил, что при 265 С ( масляная баня) время, необходимое для установления равновесия, исчисляется месяцами, при 350 С ( кипящая ртуть) - днями, при 440 С ( кипящая сера) - часами. Он нашел, что состояние равновесия этой системы не зависит от давления. [38]
Как выяснилось, в отличие от внешне похожей реакции образования йодистого водорода в данном случае кинетическое уравнение имеет довольно сложный вид. [39]
Если не так давно цепные реакции рассматривались как исключение, отклонение от нормального течения процессов, то в последние годы накапливается все больше данных для противоположного утверждения: путь через атомы и радикалы, по крайней мере, для гомогенных газовых реакций является наиболее естественным и легким путем. Известно всего лишь несколько бимолекулярных газовых процессов ( подобных образованию йодистого водорода), в то время как реакций с установленным цепным механизмом очень много. К ним относятся такие важные процессы, как горение и окисление водорода, окиси углерода, углеводородов и др. органических со-едииений хлорирование, полимеризация, крекинг и многие другие, причем перечень их все время пополняется. Среди цепных реакций разветвленные цепи встречаются гораздо реже, чем неразветвлен-ные. [40]
 |
Электролитическая ячейка прибора ГКП-1. [41] |
На дне измерительной камеры под электродом всегда находится небольшое количество кристаллического иода, который медленно растворяется по мере его выдувания. Сернистый ангидрид при просасывании воздуха через электролит реагирует с иодом с образованием йодистого водорода, который затем количественно окисляется. [42]
Входящая к это уравнение константа т почти не зависит от температуры. Различие между уравнением ( 121) и простим уравнением, которое описывает скорость образования йодистого водорода, является разительным примером, свидетельствующим о многообразии яплений, встречающихся в химической кинетике, и о трудности их теоретического объяснения только на основе аналогий без достаточного фактического материала. [43]
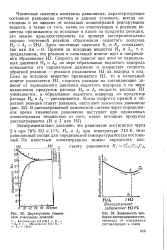 |
Двустороннее химическое равновесие реакций.| Зависимость изо-барно-изотермического потенциала от содержания составляющих в смеси. [44] |
Примем за исходные вещества Н2 и Ja T - е-предположим, что реакция в начальный момент идет в направлении образования HJ. Скорость ее зависит при этом от парциальных давлений Н2 и J2; по мере образования йодистого водорода повышается его парциальное давление и возрастает скорость обратной реакции - реакции разложения HJ на водород и иод. Если за исходное вещество принимается HJ, то в начальный момент разлагается HJ, скорость распада на составляющие зависит от парциального давления йодистого водорода и по мере накопления продуктов распада Н2 и J2 скорость распада HJ уменьшается, а образование йодистого водорода из продуктов распада Н2 и J2 - увеличивается. [45]
Страницы: 1 2 3 4