Образование - цианистый водород
Cтраница 2
Из новых направлений представляет интерес образование цианистого водорода при очень высоких температурах ( 3000 - 4000), достигаемых при адиабатическом сжатии исходных газов до 5 - 10 тыс. ат или развиваемых в плазменных реакторах. [16]
Исследования [43] показывают, что образование цианистого водорода при термоокислительном разложении пенополиуретанов рецептур 304Н и 9Н зависит от скорости нагревания материала и расхода воздуха, причем с уменьшением скорости нагревания и увеличением расхода воздуха на термоокислительное разложение образование цианистого водорода увеличивается. [17]
Существуют различньш представления о механизме образования цианистого водорода при неполном окислении метана и аммиака на катализаторе. [18]
Существуют различные представления о механизме образования цианистого водорода при неполном окислении метана и аммиака на катализаторе. [19]
Благодаря присутствию угольной кислоты удается избежать образования цианистого водорода и окрашивания раствора дициана в коричневый цвет. [20]
Из совершенно новых направлений представляет интерес образование цианистого водорода при адиабатическом сжатии96 до 5 - 10 тыс. атм смесей СН4 N2 Аг и С2Н2 N2 Ar. Добавки Аг способствуют повышению температуры, развиваемой при сжатии. Максимальный выход HCN равен 1 % от начального объема смеси, содержащей 10 % СН4, 13 % N2, 77 % Аг при давлении 8500 атм и 4 % для смеси 25 % С2Н2, 32 % N2 43 % Аг при давлении 7400 атм. [21]
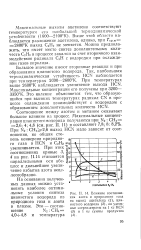 |
Влияние соотношения азота и природного газа на выход ацетилена ( /, цианистого водорода ( 2, на удельные энергозатраты на 1 кг HCN ( 3 и 1 кг суммы продуктов ( 4. [22] |
Большое значение имеют вторичные реакции и при образовании цианистого водорода. Так, наибольшая термодинамическая устойчивость ИСМ наблюдается при температурах 2000 - 2600 К. При температурах выше 2600 К наблюдается увеличение выхода HCN. Максимальные концентрации его получены при 3200 - 3350 К. [23]
В местах работы с цианистыми соединениями во избежание образования цианистого водорода не допускается хранение кислот или работа с ними. Поэтому декапировочные и другие кислотные ванны должны быть изолированы от цианистых ванн. [24]
Равновесие реакции ( 6) сдвинуто в неблагоприятную для образования цианистого водорода сторону. При 450 Кр равно 0 00048, что соответствует приблизительно 2 % - ному превращению при условии, если окись углерода и аммиак взяты в эквимолярных количествах. Кроме того, цианистый водород может гидролизоваться водой, выделяющейся при реакции. Оба указанных недостатка можно частично преодолеть, используя большой избыток окиси углерода. [25]
Равновесие реакции ( 6) сдвинуто в неблагоприятную для образования цианистого водорода сторону. При 450 / Ср равно 0 00048, что соответствует приблизительно 2 % - ному превращению при условии, если окись углерода и аммиак взяты в эквимолярных количествах. Кроме того, цианистый водород может гидролизоваться водой, выделяющейся пр-и реакции. Оба указанных недостатка можно частично преодолеть, используя большой избыток окиси углерода. [26]
С показало, что 70 % общего количества азота участвует в образовании цианистого водорода. [27]
Как видно из этих данных, при пиролитическом разложении большого числа азотсодержащих органических соединений происходит образование цианистого водорода, поэтому отрицательная проба на ионы цианида может характеризовать природу соединения. То же относится к относительно редким случаям обнаружения в продуктах пиролиза дициана и ацетальдегида. [28]
Вентиляционные установки местных отсосов от ванн с цианистыми и кислыми растворами должны быть самостоятельными во избежание образования цианистого водорода при взаимодействии ( смешивании) цианистых соединений с кислотами. [29]
В последнее время в патентной литературе опубликованы многочисленные работы по промышленному внедрению высокотемпературных процессов, ведущих к образованию цианистого водорода. Большинство этих процессов основано на использовании частичного окисления метана кислородом или воздухом как источника тепла для взаимодействия основного количества метана с аммиаком. Иногда [8, 46] реакция осуществляется без катализатора, но значительно чаще применяют катализаторы, подобные используемым в процессе частичного окисления аммиака до азотной кислоты. При использовании сульфидов [36] или меркаптанов [23] выход цианистого водорода увеличивается. Температура синтеза обычно не превышает 1600 К. Предложены также двухступенчатые процессы [12, 38], основанные на получении окиси азота частичным окислением аммиака, с последующим взаимодействием ее с углеводородами, ведущим к образованию цианистого водорода. [30]
Страницы: 1 2 3 4