Образование - трехокись - сера
Cтраница 1
Образование трехокиси серы в электрическом разряде изучено еще менее полно, чем при облучении. [1]
Образование трехокиси серы в продуктах сгорания отражается на температуре, при которой происходит конденсация на охлажденных поверхностях, соприкасающихся с газами, или на так называемой точке росы. В качестве конденсата образуется серная кислота, концентрация которой зависит от влажности топочных газов. Вследствие зависимости между упругостью пара и температурой этой кислоты точка росы будет обычно значительно выше, чем можно было ожидать, исходя только из содержания водяного пара в газах. [2]
Образование трехокиси серы в электрическом разряде изучено еще менее полно, чем при облучении. Это связано со сложностью процесса; окисление двуокиси серы в разряде может осуществляться при взаимодействии возбужденных ударами электронов молекул двуокиси серы или кислорода, а также в результате образования озона, окислов азота и другими путями. [3]
Так как образование трехокиси серы сопровождается выделением тепла, то равновесный выход ее или степень окисления двуокиси серы с повышением температуры уменьшается. [4]
Чтобы предотвратить образование трехокиси серы по газовому тракту и снизить потери серы в печном отделении, необходимо подавать в печь минимально возможное количество воздуха. Газовый тракт, в том числе электрофильтр, должен быть тщательно герметизирован, так как повышение содержания кислорода в обжиговом газе способствует образованию серного ангидрида. Рекомендуется также резкое охлаждение газа после печи до температуры 450 С. [5]
Вопросу о том, как свести к минимуму образование трехокиси серы и окислов азота в процессах горения, посвящено огромное число работ. [6]
Предварительная обработка полученных результатов показала, что скорость образования трехокиси серы удовлетворительно передается уравнением ( 11 7), константы же kz, вычисленные по уравнению ( II, 8) из опытов по разложению трехокиси серы, заметно уменьшаются с повышением концентраций двуокиси серы и кислорода. Поскольку опыты были поставлены только с газовыми смесями стехиометрического состава, нельзя было непосредственно установить, который из этих газов снижает скорость разложения трехокиси серы. [7]
Предварительная обработка полученных результатов показала, что скорость образования трехокиси серы удовлетворительно передается уравнением ( 11 7), константы же / г2, вычисленные по уравнению ( II, 8) из опытов по разложению трехокиси серы, заметно уменьшаются с повышением концентраций двуокиси серы и кислорода. Поскольку опыты были поставлены только с газовыми смесями стехиометрического состава, нельзя было непосредственно установить, который из этих газов снижает скорость разложения трехокиси серы. [8]
Излучения с длиной 2537 А и выше не вызывают образования трехокиси серы, хотя и поглощаются двуокисью серы. [9]
С понижением температуры равновесие реакции окисления SO2 в SO3 смещается в сторону образования трехокиси серы. [10]
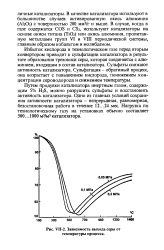 |
Зависимость выхода серы от температуры процесса. [11] |
Избыток кислорода в технологическом газе перед вторым конвертором приводит к сульфатации катализатора в результате образования трехокиси серы, которая соединяется с алюминием, входящим в состав катализатора. Сульфаты снижают активность катализатора. Сульфатация - обратимый процесс, она возрастает с повышением кислорода, понижением концентрации сероводорода и снижением температуры. [12]
 |
Контактный аппарат. [13] |
Поскольку реакция ( V, 17) обратима, начинают процесс при высокой температуре для обеспечения высокой скорости и постепенно снижают ее для сдвига равновесия в сторону образования трехокиси серы. Этому способствует специальное оформление конструкции контактного аппарата. [14]
Таким образом экспериментально доказано, что взаимодействие двуокиси серы с пятиокисью ванадия, приводящее к образованию кристаллических продуктов, нельзя рассматривать как этап каталитического окисления, а сульфат ванадила не является промежуточным продуктом при окислении двуокиси серы на чистой пятиокиси ванадия, так как скорость его образования гораздо меньше скорости образования трехокиси серы. Малую каталитическую активность чистой пятиокиси ванадия нельзя объяснить легкостью перехода ее в сульфат ванадила, а следует считать характерной для самого вещества. [15]
Страницы: 1 2