Образование - азеотроп
Cтраница 1
Образование азеотропов является следствием межмолекулярного взаимодействия, приводящего к отклонению поведения компонентов растворов от идеального. Поэтому предсказание явления азеотропии обусловлено возможностью количественного определения указанных отклонений по данным о свойствах компонентов. Это центральная задача теории растворов, решенная лишь для отдельных частных случаен. Имеется, однако, ряд эмпирических обобщений, полезных для решения обсуждаемого вопроса. [1]
Образование азеотропов оказывает определяющее влияние на условия разделения жидких смесей методами дистилляции и ректификации. [2]
 |
Взаимное расположение дистилляционной линии ( / и линии пара ( 2. [3] |
Образование азеотропов в трехкомпонентной системе обусловливает усложнение зависимости температуры кипения смесей от состава. На поверхности температур кипения появляются вмятины или возвышения, могущие вызвать образование нескольких семейств изотерм-изобар. [4]
При образовании азеотропа с максимальной температурой кипения в дистиллате получают чистый компонент, а в кубовом продукте - смесь обоих компонентов. [5]
При образовании азеотропа с максимальной температурой кипе ния в дистиллате получают чистый компонент, а в кубовом про дукте - смесь обоих компонентов. [6]
 |
Зависимость давления ( а и состава пара ( б от состава жидкости в бинарных системах с положительным ( т и отрицательным ( М азеотропами. [7] |
Рауля возможно образование азеотропа и тем ближе его состав к эквимолекулярной смеси. [8]
Однако из-за образования азеотропа фенола с ацетофеноном выделение чистого фенола ректификацией невозможно. Разложением аммиачной соли фенола выделяют 95 % фенола, находящегося в фенольной смоле. [9]
В случае образования азеотропа с минимальной температурой кипения дистнллат представляет собой смесь обоих компонентов, кубовый остаток - один чистый компонент. [10]
В случае образования азеотропа с минимальной температурой кипения дистиллат представляет собой смесь обоих компонентов, кубовый остаток - один чистый компонент. [11]
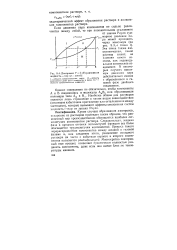 |
Диаграмма Т f ( Л / равновесия жидкость - пар ( р const. [12] |
Кроме случаев образования азеотропов, испарение из растворов протекает таким образом, что равновесный пар преимущественно обогащается наиболее легколетучим компонентом раствора. Следовательно, жидкая фаза в процессе отгонки легколетучей фракции все более обогащается труднолетучим компонентом. Процесс такого перераспределения компонентов между жидкой и газовой фазами и, как следствие этого, разделение исходного раствора на части с избытком первого и второго компонентов называется ректификацией. Многократно повторенный этот процесс позволяет практически полностью разделить компоненты, даже если они имеют близкие температуры кипения. [13]
В ряде случаев образование азеотропа является нежелательным, как это имеет место, например, при концентрировании смеси этиловый спирт - вода и др. В других же случаях это дает возможность разрушить уже имеющийся азеотроп и разделить близкокипящую смесь. Специальная добавка так называемого выносителя ( Schleppmittel) приводит к образованию нового азеотропа между ним и одним из компонентов двойной смеси; этот новый азеотроп должен быть легче отделим от второго компонента вследствие большей разницы их температур кипения. Необходимым условием является легкость последующего разделения сконденсированного азеотропа на составные части, что достигается охлаждением, высаливанием2), химическим отделением добавленного вещества, экстракцией компонента, который необходимо выделить, или же дополнительной азеотропной ректификацией. [14]
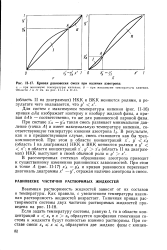 |
Кривая равновесия смеси при наличии азеотропа. [15] |
Страницы: 1 2 3 4