Образование - цианамид
Cтраница 2
Механизм реакции Халлера - Бауэра, предложенный Фрей-длиным [6] для случая взаимодействия расплавленной эвтектической смеси амидов натрия и калия с кетоном или амидом, приведен ниже. Расщепление происходит с выделением карбонильной группы и образованием цианамидов металлов. [16]
Порошок темно-серого цвета, почти нерастворимый в воде. В слабо кислой среде происходит распад его с образованием цианамида водорода, мочевины, аммиака, нитритов и нитратов. [17]
При температуре 300 - 600 С примеси цианата, цианида и карбоната к цианамиду кальция присутствуют в значительном количестве. Характерной особенностью полученных зависимостей является то, что начало образования цианамида и карбоната сдвинута во времени по отношению к цианиду и цианату. [18]
Цианамид может образовывать нерастворимые соли с тяжелыми металлами, что также приведет к смещению равновесия вправо. Однако для простоты изложения предлагаемого термодинамического анализа условий осаждения сульфидов рассмотрим случай, когда образование цианамида металла не происходит. Такое допущение справедливо для многих систем, в которых ион металла связан в достаточно прочное комплексное соединение. [19]
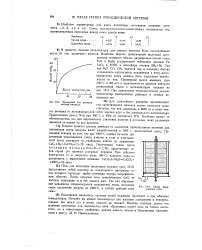 |
Примерный ход реакции синтеза аммиака.| Схема циан-амидной печи. [20] |
Печь для получения цианамида кальция ( рис. IX-6) представляет собой цилиндр из огнеупорного материала, по оси которого проходит труба, имеющая внутри нагревательную обмотку. После загрузки печи измельченным СаСа ее наглухо закрывают и в нее подают азот. Так как образование цианамида сопровождается выделением тепла, исходную смесь достаточно нагреть до 1000 С, а дальше реакция идет сама. [21]
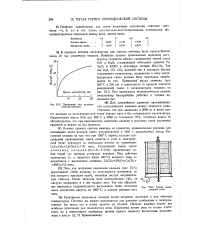 |
Примерный ход реакции синтеза аммиака.| Схема циан-амидной печи. [22] |
Печь для получения цианамида кальция ( рис. IX-6) представляет собой цилиндр из огнеупорного материала, по оси которого проходит труба, имеющая внутри нагревательную обмотку. После загрузки печи измельченным СаС2 ее наглухо закрывают и в нее подают азот. Так как образование цианамида сопровождается выделением тепла, исходную смесь достаточно нагреть до 1000 С, а дальше реакция идет сама. [23]
В водных растворах превращается в циануровую кислоту. Разлагается при 600 с образованием цианамида. [24]
Темно-серый, почти черный, пылящий, плохо растворимый в воде порошок с запахом ацетилена. Содержит 17 - 19 % азота и 1 - 1 5 % минерального масла. В почве разлагается с образованием цианамида юдорода, мочевины, аммиака, нитратов и нитритов. На сорняки губительное действие оказывают нитриты и цианамид водорода. [25]
Мало растворим в спирте; нерастворим в большей части органических растворителей. С кислотами образует соли, в водных растворах превращается в циануровую кислоту. Легко взаимодействует с альдегидами. Разрушается при температуре около 600 с образованием цианамида. [26]
 |
Схема циан-амидыой печи. [27] |
Значительно меньшее промышленное значение имеет разработанный в 1901 г. цианамидный метод. Последний основан на том, что при высоких температурах карбид кальция ( получаемый накаливанием смеси извести и угля в электрической печи) реагирует со свободным азотом по уравнению CaC2 N2CaCN2 C 70 / скал. Полученный таким путем цианамид кальция ( Ca N-CsN) представляет собой серый ( от примеси углерода) порошок. Она представляет собой цилиндр из огнеупорного материала, по оси которого проходит труба, имеющая внутри нагревательную обмотку. После загрузки печи измельченным СаС2 она наглухо закрывается и в нее подается азот. Так как образование цианамида сопровождается выделением тепла, исходную смесь достаточно нагреть до 800 С, а дальше реакция идет сама. [28]
Значительные успехи были достигнуты Франклином [6] при применении концепции сольвосистем к азотным производным угольной кислоты. Ему удалось показать, что такие вещества, как карбами-новая кислота, мочевина и гуанидин, являются азотными аналогами угольной кислоты ( аммоноугольными кислотами) и что все они ведут себя как кислоты в жидком аммиаке, несмотря на то, что в воде химический характер этих соединений очень сильно различается. Образование этих трех аммонопроизводных угольной кислоты осуществляется при помощи реакции сольволиза или сольватации. Так, например, при соединении двуокиси углерода и аммиака получается аммониевая соль карбаминовой кислоты; хлорангидрид угольной кислоты, фосген, реагируя с аммиаком, образует мочевину. Первая из этих реакций является реакцией сольватации; вторая - реакцией сольволиза. Четыреххлористый углерод, хлорангидрид неизвестной ортоугольной кислоты, подвергается реакции аммоно-лиза, превращаясь в результате взаимодействия с аммиаком непосредственно в гуанидин. Примером реакции десольватации может служить превращение аммониевой соли карбаминовой кислоты в мочевину или в циановую кислоту. Мочевина может дегидратироваться с образованием цианамида, который, с точки зрения Франклина, также является аммоноугольный кислотой. С другой стороны, цианамид может быть превращен в гуанидин как при действии иона аммония в жидком аммиаке, так и при сплавлении с солью аммония при высоких температурах; обе эти реакции представляют собой реакции сольватации. [29]
Страницы: 1 2