Образование - цирконат
Cтраница 1
 |
Фазовые отношения в системе СаО - Zr02 ( по Кокко.| Параметры кристаллической решетки кубических твердых растворов системы СаО - Zr02 ( по Кокко. [1] |
Образование цирконата протекает с большой скоростью при 1000 - 1200, тогда как для получения твердых растворов требуются значительно более высокие температуры. [2]
Образование цирконата самария ( Sm2Zr207 со структурой типа пирохлора) при температурах 1200 - 1300 С протекает по аналогичному механизму. [3]
Экзотермический эффект образования цирконата кальция на термограмме совпадает с мощной эндотермикой диссоциации карбоната кальция, а полиморфное превращение двуокиси циркония сопровождается на термограмме глубоким эндотермическим эффектом с максимумом при 1170 С. [4]
В интервале 700 - 800 С образование цирконата кальция происходит довольно быстро и сопровождается возрастанием электросопротивления. Причина большой скорости протекания процесса в твердой фазе заключается в том, что продукт реакции не образует плотного слоя вокруг зерен двуокиси циркония ( из-за большого различия в молекулярных объемах) и некоторое время не оказывает значительного препятствия доставке реагирующих компонентов, друг к другу. [5]
При сплавлении циркона с NaOH протекают реакции образования цирконатов, цирконосиликатов и силикатов натрия, растворимых в воде и различных кислотах. [6]
Окислами алюминия и циркония ортоуранаты щелочноземельных металлов разлагаются с образованием цирконатов и алюминатов соответствующих щелочноземельных металлов. Такая направленность реакций говорит о том, что сила химической связи между щелочноземельным металлом и ураном в ортоуранате слабее, чем между щелочноземельным металлом и цирконием или алюминием в цирконатах и алюминатах. С другой стороны, поскольку эксперимент показывает, что разложение ортоураната идет только до моноура-ната и избыток окиси алюминия или двуокиси циркония с моноуранатами не взаимодействует, прочность химической связи в моноуранатах сильнее, чем в алюминатах и цирконатах. Таким образом, если окислы алюминия и циркония нельзя рассматривать как конструкционные материалы в контакте с ортоуранатами щелочноземельных металлов, то в контакте с моноуранатами можно. [7]
Резкое уменьшение процента коллоидной формы при рН 11 - 12 связано, по-видимому, с образованием цирконатов. [8]
Резкое уменьшение процента коллоидной формы при рН 11 - 12 связано, по-видимому, с образованием цирконатов. [9]
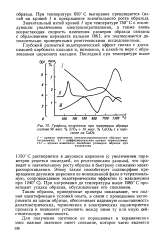 |
Графики, полученные при нагревании образца состава 90 масс. % ZrO2 10 масс. % СаСОз ( в пересчете на СаО. [10] |
Глубокий размытый эндотермический эффект связан с диссоциацией карбоната кальция и, возможно, в какой-то мере с образованием цирконата кальция. [11]
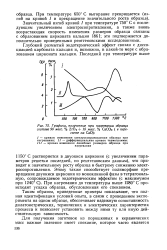 |
Графики, полученные при нагревании образца состава 90 масс. % ZrO2 10 масс. % СаСОз ( в пересчете на СаО. [12] |
Значительный изгиб кривой / при температуре 750 С с последующим увеличением электросопротивления, а также вновь возрастающая скорость изменения размеров образца связаны с образованием цирконата кальция [86 ]; это подтвержается дополнительно проведенными рентгеновскими исследованиями. [13]
А; теплота образования 20 8 ккал / моль; хорошо разлагается серной, фосфорной и плавиковой кислотами с образованием иона циркония, а щелочами - с образованием цирконатов. [14]
Взаимодействие двуокиси циркония с окисью лантана протекает значительно сложнее. Реакция взаимодействия начинается с образования цирконата лантана на поверхности частиц двуокиси циркония. Реакция заканчивается образованием цирконата лантана для состава 33.3 мол. [15]
Страницы: 1 2