Образование - гидроокись - металл
Cтраница 1
Образование гидроокиси металла, выпадающей в виде твердой фазы из раствора нейтральной соли этого металла, происходит после того, как рН раствора достигает определенного значения, которое носит название рН гидратообразования. [1]
Образование гидроокисей металлов происходит обычно в слабокислых или нейтральных средах в условиях совместного выделения металла и водорода, когда в прикатодном слое электролита становится возможным гидролиз. Образующиеся при этом коллоидные взвеси обладают характерными свойствами гелей, адсорбируются на металле и существенно влияют на структуру и свойства электролитических осадков. [2]
Образование гидроокиси металла, выпадающей в виде твердой фазы из раствора нейтральной соли этого металла, происходит после того, как рН раствора достигнет определенного значения, которое носит название рН гидратообразования. [3]
Образование гидроокисей металлов происходит обычно в слабокислых или нейтральных средах в условиях совместного выделения металла и водорода, когда в прикатодном слое электролита становится возможным гидролиз. Образующиеся при этом коллоидные взвеси обладают характерными свойствами гелей, адсорбируются на металле и существенно влияют на структуру и свойства электролитических осадков. [4]
Чем меньше величина рН образования гидроокиси металлов, тем в более кислой области они начинают сорбироваться слабокислотными ионитами. [5]
В данной работе методом потенциометрического титрования следует определить рН образования гидроокиси металла, рассчитать ПР и активную концентрацию ионов металла в растворе. [6]
Если металл неамфотерен, его дитизонат обычно не разрушается ( с образованием нерастворимой гидроокиси металла) при встряхивании раствора в органическом растворителе с - 1 М едким натром. Примером может служить кадмий, гидроокись которого лишь слабо амфотерна. Допустим, раствор в четыреххлористом углероде, 1 10 - 5 М по Cd ( HDz) 2 и 4 10 4 М по дитизону, встряхивают с равным объемом 1 М едкого натра. [7]
Так как собственная деформация 02 - катионом ослабляет его поляризующее действие на воду, образование гидроокисей металлов из их окислов должно по мере усиления поляризующего действия катиона затрудняться, а отщепление гидроокисями воды, напротив, облегчаться. Действительно, опыт показывает, что термическая устойчивость гидроокисей 8-электронных катионов всегда значительно выше, чем гораздо сильнее поляризующих 18-электронных катионов того же - заряда и близкого радиуса. Например, NaOH и КОН кипят ( соответственно при 1378 и 1270 С) без разложения, тогда как AgOH самопроизвольно распадается на Ag2O и Н2О уже при обычных температурах. [8]
Очевидно, что в случае необходимости получения окислительной формы ЭИ производство заканчивается на стадии образования гидроокиси металла и ее осаждения на поверхности катионита. Процессы отмывки и взрыхления, конечно, необходимы, но исключаются операции восстановления гидроокисей гидросульфитом натрия. При выгрузке ЭИ из производственного фильтра в тару строгой герметизации уже не требуется. [9]
В то время как в случае галогенидов тяжелых металлов отнятие галогена эпоксидной группой эпихлоргидрина идет с образованием нерастворимой гидроокиси металла и реакция может протекать в одном направлении до конца, в случае галогенкдоз металлов, дающих водорастворимые гидроокиси, устанавливается равновесие. [10]
В то время как в случае галогенидов тяжелых металлов отнятие галогена эпоксидной группой эпихлоргидрина идет с образованием нерастворимой гидроокиси металла и реакция может протекать в одном направлении до конца, в случае галогенидов металлов, дающих водорастворимые гидроокиси, устанавливается равновесие. [11]
Сточная вода из канала 13 поступает в секцию 1, где происходит растворение металла анода в воде, образование гидроокиси металла с одновременной коагуляцией примесей и флотацией их на поверхность жидкости. Установленные в секциях 2 и 3 графитовые аноды интенсифицируют процесс очистки, способствуя более тщательному выделению из сточной воды взвешенных частиц. Вертикальное расположение графитовых пластин в секции 3 позволяет увеличить поверхность контакта сточной воды с поверхностью анода для повышения эффективности обеззараживания воды. [12]
Сродство - окисей с галоидоводородными кислотами так велико, что они могут разлагать некоторые соли металлов, гидролизующиеся водой с образованием нерастворимых гидроокисей металлов или основных солей. Так, окись этилена, медленно на холоду, быстро - при нагревании, расщепляет концентрированный раствор хлористого магния с образованием гидрата оклей магния. [13]
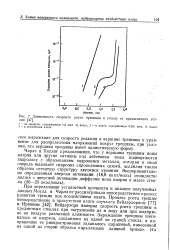 |
Зависимость скорости роста трещины в стекле от прилагаемого усилия. [14] |
Чарлз и Хиллиг ( Предположили, что у вершины трещины ионы натрия или другие катионы под действием воды подвергаются гидролизу с образованием гидроокиси металла, которая в свою очередь вызывает гидролиз еилоксановых связей, ослабляя таким образом сетчатую структуру двуокиси кремния. [15]
Страницы: 1 2