Образование - перекисная группа
Cтраница 1
Образование перекисных групп в макромолекуле поливинилового спирта непосредственным окислением его гидроксилов кислородом и даже озоном, невозможно. Как показали Н. А. Платэ, В. П. Шибаев и В. А. Каргин, в этом случае реакция протекает трудно, и необходимого для прививок количества макромолеку-лярного инициатора получить не удается. [1]
Образование перекисных групп в макромолекуле поливинилового спирта непосредственным окислением его гидроксилов кислородом и даже озоном, невозможно. Ai Плата, В. П. Шибаев и В. А. Каргин, в этом случае реакция протекает трудно, и необходимого для прививок количества макромолеку-лярного инициатора получить не удается. [2]
Образование оксидных и перекисных групп имеет важное значение при рассмотрении химизма процесса. Валентные колебания Me-О проявляются вблизи 760, 890 и 1070 см-1. Образование их и осаждение на алмазных частицах во многом защищает их от окисления. [3]
При повышенной температуре значительно ускоряется образование перекисных групп Образуются карбонильные и карбоксильные группы. Образование инородных функциональных групп по имеющимся данным способствует термоокислительному распаду. Удаление пизкомолекулярных фракций имеющих более высокое содержание карбоксильных групп обработкой горячей водой или водно-ацетоновой смесью, повышает термостабильность ацетатов целлюлозы. Перевод карбоксильных групп ( - СООН) в солевую форму за счет замещения щелочноземельными элементами Mg: и Са2 повышает стабильность ацетата целлюлзы к воздействию высоких температур. [4]
Увеличение содержания кислорода происходит вследствие образования гидроксильных и стабильных перекисных групп, а также простых и сложных эфиров. [5]
Способность некоторых лейкосоединений антрахинона к образованию перекисных групп при окислении их кислородом, равно как и способность этих перекисных групп к вторичным реакциям, например с отщеплением ШОг, были уже известны и р а мыле. [6]
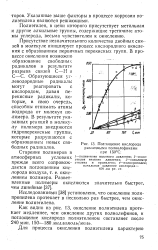 |
Поглощение кислорода. [7] |
Присутствие незначительного количества двойных связей в молекуле инициирует процесс кислородного окисления с образованием первичных перекисных групп. В процессе окисления возможно образование свободных радикалов в результате разрыва связей С - Н и С-С. Образующиеся углеводородные радикалы могут реагировать с кислородом, давая пе-рекисные радикалы, которые, в свою очередь, способны отнимать атомы водорода от молекул полимера. [8]
По этому методу полимерные вещества облучают на воздухе или в среде кислорода с целью образования перекисных групп. Эти перекисные группы достаточно устойчивы, и полимер может сохраняться на холоде, не теряя активности. Если в дальнейшем полимер нагревают в присутствии жидкого мономера или его паров до 150 С в отсутствие воздуха, перекисные группы разлагаются, образуя свободные радикалы, способные инициировать привитую полимеризацию. [9]
На воздухе эти глицериды претерпевают ряд сложных химических превращений, до сих пор до конца не изученных, несмотря на длительные и интенсивные исследования в этой области. И все-таки совершенно очевидно, что окисление глицеридов проходит через стадию образования перекисных групп, инициирующих процессы полимеризации. Механизм высыхания большей части декоративных красок представляется комбинированным: с одной стороны, испаряются растворители, с другой, происходит ауто-окисление. [10]
На воздухе эти глицериды претерпевают ряд сложных химических превращений, до сих пор до конца не изученных, несмотря на длительные и интенсивные исследования в этой области. И все-таки совершенно очевидно, что окисление глицеридов проходит через стадию образования перекисных групп, инициирующих процессы полимеризации. Механизм высыхания большей части декоративных красок представляется комбинированным: с одной стороны, испаряются растворители, с другой, происходит ауто-окисление. [11]
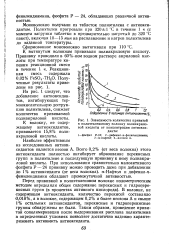 |
Зависимость количества привитой к полиэтиленовому волокну полиакриловой кислоты от концентрации антиоксиданта. [12] |
Наиболее эффективным из исследованных антиоксидантов является неозон А. Всего 0 2 % ( от веса волокна) этого антиоксиданта полностью ингибирует образование перекисных групп в полиэтилене и последующую прививку к нему полиакриловой кислоты. Нафтол и дифенил-п-фенилендиамин обладают промежуточной активностью. [13]
Двуокись титана способна поглощать ультрафиолетовые лучи, что может привести к фотовосстановлению TiO2 с выделением кислорода или озона, которые могут окислять органические компоненты бумаги. Это объясняется тем, что атом титана, входящий в двуокись, может посредством координационной связи прочно присоединять две молекулы воды с образованием перекисной группы в виде напряженного треугольного цикла, которая неустойчива и разлагается с выделением озона и кислорода. [14]
Теория Энглера была единственной признаваемой в течение 40 лет, хотя подтвердить ее экспериментально не представлялось возможным. Она дает объяснение уменьшению йодного числа, наблюдаемому при окислении льняного и других высыхающих масел: в начальной стадии окисления йодное число по мере образования перекисных групп уменьшается так, что одна молекула иода соответствует одной молекуле присоединившегося активного кислорода. Таким образом, на каждую образовавшуюся перекисную группу должна исчезнуть одна двойная связь. Это соотношение справедливо только в узком промежутке времени в самом начале процесса окисления, так как экспериментально найдено, что йодное число монотонно уменьшается, тогда как перекисное число сначала стабилизируется, а затем тоже начинает уменьшаться. Эти экспериментальные данные не подтверждают, таким образом, предложенной теории. [15]
Страницы: 1 2