Обрыв - цепная реакция
Cтраница 2
Образование последних происходит, очевидно, за счет превращений, приводящих к обрыву цепной реакции. [16]
Механизм действия антиоксидантов, по крайней мере для случая вторичных аминов, сводится к обрыву цепной реакции по причине возникновения вместо активных радикалов RO - nRO2 - малоактивных радикалов, стабилизованных вследствие так называемого эффекта сопряжения. Это обстоятельство позволяет наметить пути синтеза антиоксидантов высокой эффективности. [17]
Механизм действия антиоксидантов, по крайней мере для случая вторичных аминов, сводится к обрыву цепной реакции по причине возникновения вместо активных радикалов RO - HRO2 - малоактивных радикалов, стабилизованных вследствие так называемого эффекта сопряжения. Это обстоятельство позволяет наметить пути синтеза антиоксидантов высокой эффективности. [18]
Так как концентрация [ К - ] значительно меньше концентрации [ КОО - ], тс обрыв цепной реакции протекает чаще всего по последней схеме. [19]
Антиокислитель эффективен в окисляющейся системе в очень малых концентрациях, так как его действие основано на обрыве цепной реакции. Продолжительность этого действия зависит от химической природы антиокислителя и судьбы его молекулы в окисляющейся системе. Радикалы антиокислителя могут рекомбиниро-ваться до исходной молекулы; еще больший эффект достигается, если продукты окисления также являются ингибиторами. [20]
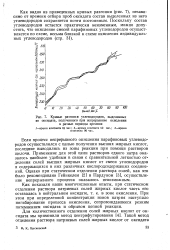 |
Кривые разгонки углеводородов, выделенных. [21] |
При этом при определенной концентрации ионов натрия наступало ингибирование процесса окисления, сопровождавшееся резким потемнением оксидата и обрывом цепной реакции. [22]
Поглощение нейтронов ядрами 92U235 способствует развитию цепной реакции, поглощение же их ядрами U238 выводит нейтроны из цепной реакции и ведет к обрыву цепной реакции. Расчеты показывают, что в естественной смеси изотопов урана вероятность обрыва цепной реакции превышает вероятность развития реакции и цепная реакция деления не может развиваться ни на быстрых, ни на медленных нейтронах. [23]
Повышение каталитической активности цеолитсодержащего катализатора, температуры при одновременном увеличении массовой скорости подачи сырья и сохранении постоянной глубины превращения способствует десорбции промежуточных продуктов реакции уплотнения, обрыву цепной реакции зарождения и уменьшению инициированной, цепной реакции образования на активных центрах твердых полимеров кокса. По мере утяжеления сырья, роста его коксогенности требуется все большая интенсификация процесса путем одновременного повышения температуры и сокращения продолжительности контакта сырья с катализатором. При сохранении глубины процесса постоянной наблюдается уменьшение выхода кокса на 20 - 30 % и повышение выхода остальных продуктов. На многих заводах каталитическому крекингу подвергают мазуты и гудроны, содержащие до 50 млн металлов при температуре в низу лифт-реактора 600 С и продолжительности контактирования не более 2 с. Дальнейшая интенсификация процесса сдерживается ростом доли реакций термического крекинга, выхода сухого газа и ослаблением реакций Н - переноса. [24]
Наблюдаются три стадии процесса: 1) инициирование - образование свободных макрорадикалов под нагрузкой; 2) развитие вторичных реакций ( превращения макрорадикалов); 3) обрыв цепных реакций и гибель активных центров. [25]
Одновременно с указанными реакциями могут также идти и другие, но их значение в общем развитии процесса несущественно, хотя при определенных условиях, например постоянной температуре и давлениях до 0 5 кПа, они могут привести к обрыву цепной реакции. [26]
Тем самым радикальная цепь обрывается полностью. Обрыв цепной реакции может происходить также в результате переноса цепи. [27]
Полученные данные объясняются следующим образом: карбопды являются псевдокристаллитами, размеры и состав которых соответствуют условиям процесса. Они являются продуктами рекомбинации и обрыва цепной реакции уплотнения. Обнаруженные в кароопдах неспаренные электроны ( 1020 - 1021) принадлежат к стабильным радикалам, сильно делокализованы, экранированы, скрыты и в условиях нроцесса слабо доступны. [28]
Согласно мнению Ларсена и Даймонда [37], роль антиокислителей могут выполнять либо ингибиторы, либо замедлители окисления. Действие ингибиторов окисления состоит в обрыве цепной реакции; замедлители превращаются в ингибиторы в процессе окисления. [29]
Следует отметить, что в реакции водорода с кислородом не происходит тройных молекулярных столкновений и все стадии осуществляются в результате простых, бимолекулярных столкновений, т.е. являются реакциями второго порядка. Интересно также и то, что обрыв цепной реакции происходит только на стенках сосуда. По этой причине не следует забывать, что сосуд - неотъемлемая часть реакционной системы и что вещество, из которого он изготовлен, может оказывать большое влияние на протекание реакции. [30]
Страницы: 1 2 3 4