Объемный обрыв - цепь
Cтраница 2
Частота процессов, приводящих к обрыву цепей, Уг либо остается без изменения, либо может расти в результате накопления образующихся в ходе реакции веществ, способствующих обрыву цепей. Так, например, в реакции горения водорода вероятность объемного обрыва цепей увеличивается по мере образования воды, так как молекулы воды являются более эффективным партнером приводящего к объемному обрыву цепей тройного соударения Н 02 Н20 Н20 - f - H02, нежели молекулы водорода или кислорода. [16]
Обрыв цепей связан с исчезновением активных центров вследствие химических реакций, развивающихся при участил атомов и радикалов. Эти реакции могут протекать и в объеме и на поверхности раздела. Объемный обрыв цепей иногда сводится к рекомбинации свободных атомов и радикалов. [17]
Диффузионная и кинетическая области реакции. Наряду с объемным обрывом цепей небходимо учитавать также обрыв цепей на стенках реакционного сосуда. Обрыв цепей на стенках становится доминирующим при низких давлениях. [18]
Допустим, реакция протекает в диффузионной области, причем зарождение цепей происходит в объеме, но обрыв цепей допускается как в объеме, так и на стенках сосуда. Предполагается далее, что объемный обрыв цепей следует линейному закону. Пусть реакция протекает в плоском сосуде. [19]
Кинетика цепной химической реакции, ее скорость и средняя длина цепи, естественно, находятся в прямой связи с условиями протекания реакции и в первую очередь с условиями зарождения и обрыва цепей. Здесь мы рассмотрим вопрос о скорости стационарной реакции, ограничившись случаем, когда цепи зарождаются в объеме, но допуская обрыв цепей как в объеме, так и на поверхности. При этом будем считать, что объемный обрыв цепей следует линейному закону и что реакция протекает в диффузионной области. [20]
Кинетика цепной химической реакции, ее скорость и средняя длина цепи, естественно, находятся в прямой связи с условиями протекания реакции. Здесь мы ограничимся случаем, когда цепи зарождаются в объеме, но обрыв цепей происходит как в объеме, так и на поверхности. При этом будем считать, что объемный обрыв цепей следует линейному закону и что реакция протекает в диффузионной области. [21]
Кинетика цепной химической реакции, ее скорость и средняя длина цепи, естественно, находятся в прямой связи с условиями протекания реакции и в первую очередь с условиями зарождения и обрыва цепей. Здесь мы рассмотрим вопрос о скорости стационарной реакции, ограничившись случаем, когда цепи зарождаются в объеме, но допуская об ыв цепей как в объеме, так и на поверхности. При этом будем считать, что объемный обрыв цепей следует линейному закону и что реакция протекает в диффузионной области. [22]
Возрастание скорости реакции внутри области воспламенения, как было показано выше, не может быть беспредельным. Для того чтобы найти максимально возможные в данных условиях значения ( Н) и со, необходимо учесть еще выгорание исходных веществ. Такого рода расчеты были проведены Ковальским и позднее Семеновым [17] для малых давлений ( рСр2), при которых можно пренебречь скоростью реакции ( VII) объемного обрыва цепей. [23]
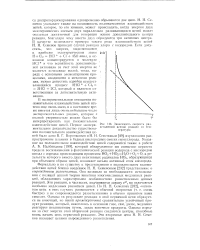 |
Зависимость скорости разветвленной цепной реакции от температуры. [24] |
В экспериментальном отношении положительное взаимодействие цепей изучено еще очень мало, и в настоящее время имеется лишь очень небольшое число экспериментальных данных, которые с полной уверенностью можно было бы интерпретировать как положительное взаимодействие цепей. Первое экспериментальное доказательство существования положительного взаимодействия цепей было дано В. Г. Воропковым и Н. Н. Семеновым [49], изучавшими распространение пламени в бедных кислородных смесях сероуглерода. Указание на положительное взаимодействие цепей содержится также в работе А. Б. Налбандяна [199], который обнаруженное им смещение верхнего предела воспламенения в фотохимической реакции водорода с кислородом связал с изредка происходящим процессом НО2 НО2 Н2О О2 О, в результате которого вместо двух неактивных радикалов НО2, образующихся при объемном обрыве цепей, возникает весьма активный атом кислорода. [25]
Страницы: 1 2