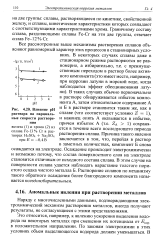
Объем - выделяющийся водород
Cтраница 2
Сколько граммов серной кислоты может вступить во взаимодействие с 14 8 г магния. Чему равен объем выделяющегося водорода. [16]
Это относится, например, к явлению ускорения выделения водорода на некоторых металлах при смещении их потенциала от Екор в положительном направлении. По законам электрохимии в этих условиях объем выделяющегося водорода должен уменьшаться. [18]
Было установлено количественное совпадение скоростей коррозии, определенных по объему выделяющегося водорода и рассчитанных на основе электрохимических измерений. Тем самым впервые было показано, что не только амальгамы, но и твердые металлы растворяются в полном соответствии с закономерностями электрохимической кинетики. [19]
 |
Влажная камера конструкции. [20] |
При определении степени коррозии металлов пользуются как весовыми, так и объемными методами. В первом случае собирают и взвешивают продукты коррозии, во втором измеряют объем выделяющегося водорода или поглощенного кислорода. [21]
Новицкой и А. А. Северова [51], что только благодаря фосфату цинка возможно ускорение пленкообразования, уменьшение тНг и объема водорода, а также фосфатирования тонкостенных, полых и проволочных изделий не подтверждается ни отечественной, ни зарубежной практикой. Наши исследования, литературные данные и накопившийся многолетний производственный опыт заводов ряда отраслей промышленности показывают, что и при использовании железомарганцовых препаратов ( мажеф, ВИМ) в сочетании с окислителями ( например, Zn ( N03) 2) достигается значительное ускорение в 10 - 12 раз образования фосфатной пленки и резко сокращается объем выделяющегося водорода. [22]
Как следует поступить, чтобы площадь поверхности была постоянной. Измерьте скорость растворения ( по объему выделяющегося водорода) в растворах соляной кислоты различной концентрации, например 1 М; 0 5 М, 0 25 М или др. Приводит ли уменьшение концентрации ионов водорода, скажем, в 2 раза к уменьшению скорости реакции в 2 раза. Зависит ли он от площади поверхности и концентрации кислоты. [23]
Образец смешивают со спиртовым раствором борной кислоты, добавляют 3 мл 0 13 М раствора борогидрида натрия в растворе гидроокиси натрия. После завершения реакции избыток борогидрида натрия разлагают серной кислотой и измеряют объем выделяющегося водорода. [24]
Полученный указанным методом гидрид лития анализируют спектрографически на присутствие других щелочных металлов и кальция. Согласно анализу, содержание этих металлов составляет менее чем 100 / 1000 000 вес. Водород в гидриде определяют обработкой иавески смесью воды с диоксаном и измерением объема выделяющегося водорода. [25]
 |
Реакционный сосуд для определения карбонильной группы по Соботке и. [26] |
Навеску помещают в отросток /, в отросток 2 точно отмеривают с помощью ультрамикропипетки 0 1 мл 0 3 М раствора борогидрида натрия в диглиме, а в отросток 3 вводят 1 5 мл раствора хлористого водорода в пропаноле. В конце реакции раствор из отростка 3 переводят в отросток / и измеряют объем выделяющегося водорода. Ма и Штейнталем 205 разработана простая методика, в которой в качестве реагента ( см. пример 33 в гл. [27]
 |
Прибор для определения глубины коррозионных поражений. [28] |
Протекание коррозионного процесса во времени наблюдают обычно при периодическом отборе части испытуемых образцов. Кинетику коррозии металлов с водородной или кислородной деполяризацией можно исследовать непрерывно при помощи объемных показателей, применяя для этого объемные методы. На рис. 335 приведен общий вид установки для определения скорости коррозии металлов с водородной деполяризацией по объему выделяющегося водорода. Заполнение бюреток в начале опыта и при их периодической перезарядке в процессе испытания осуществляется засасыванием коррозионного раствора с помощью водоструйного насоса. [29]
Существует ряд способов исследования антикоррозионных свойств покрытий: погружение образцов в неподвижный или движущийся электролит, испытание образцов во влажной камере, с распылением корродирующего раствора, в газовой среде, содержащей корродирующие компоненты и, наконец, электрохимические методы. Степень коррозии металла в этих испытаниях определяют количественно весовыми и объемными методами. При весовом методе степень коррозии определяют взвешиванием металлического образца до покрытия защитной пленкой и после испытания и удаления пленки. Объемный способ определения степени коррозии заключается в измерении объема выделяющегося водорода или поглощенного кислорода при испытании образца. [30]
Страницы: 1 2 3