Мольный объем
Cтраница 2
Мольный объем - термодинамическое свойство, но мы рассматриваем исследования, касающиеся объемных отношений в солевых системах, не в предыдущей статье, а в настоящей. [16]
Мольный объем, паровой фазы рассчитывается по уравнению состояния при известных температуре, давлении и составе. [17]
Мольный объем при комнатной температуре - это одна из первых физических величин, для которой был предложен метод групповых вкладов. [18]
Мольные объемы л с и ц / д представляют собой отношение молекулярного веса к удельному весу t - ro компонента. [19]
Мольный объем при комнатной температуре - это одна из первых физических величин, для которой был предложен метод групповых вкладов. [20]
Мольные объемы и высших ацетиленовых углеводородов рассчитаны по их критическим параметрам с помощью уравнения Ван-дер - Ваальса и составляют ( в л / моль): 22 04 -для метилацетилена; 21 9 -для винилацетилена; 21 9 -для диаце-тилена. [21]
 |
Приближенные оценки мольного объема и коэффициента теплового расширения критического комплекса а для реакции между йодистым этилом и пиридином. [22] |
Мольные объемы были определены лишь в немногих случаях, причем, по всей вероятности, парциальные мольные объемы растворенного вещества в растворе и в чистом состоянии не совпадают. [23]
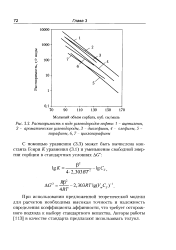 |
Растворимость в воде углеводородов нефти. 1 - ацетилены. [24] |
Мольный объем сорбата, куб. [25]
Мольный объем Ъ отвечает учетверенному суммарному объему молекул. [26]
Мольные объемы кислорода и окиси углерода записаны без индекса, поскольку, как указано выше, они принимаются одинаковыми. [27]
Мольный объем газа равен 36 л / моль. [28]
Мольный объем раствора можно также определить, используя величины, относящиеся к молю, а не молекуле. [29]
Мольные объемы VA и VB представляют собой сумму атомных объемов элементов, из которых состоят молекулы диффундирующих веществ. [30]
Страницы: 1 2 3 4