Мольный объем - смесь
Cтраница 1
Мольный объем смеси М - величина, вычисляемая по формуле. [1]
Изменения парциального мольного объема компонента раствора АУ4 и мольного объема смеси А У равны нулю, так как образование идеального раствора происходит без изменения объема. [2]
Изменения парциального мольного объема компонента раствора AV и мольного объема смеси А1 / равны нулю, так как образование идеального раствора происходит без изменения объема. [3]
Константы для отдельных газов берутся при температуре и мольном объеме смеси. Из различных сочетаний уравнений ( 120) - ( 123) с уравнением ( 119) получаются четыре различных уравнения состояни для смеси. Джиллиленд, проверивший все четыре метода по данным сжимаемости, нашел, что сочетание констант посредством уравнений ( 121) и ( 123), которое он называет аддитивностью внутренних давлений, дало наилучшие результаты. [4]
 |
Установка для исследования диффузии в газах. [5] |
Кроме того, для вычисления коэффициента диффузии были определены мольные объемы смесей. [6]
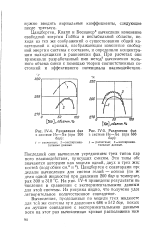
Как видно на рисунке, максимум изотерм А У ( отклонение мольного объема смеси от аддитивного) для обеих систем приходится на концентрации амида 33 % мольн. [7]
V, N () равна величине давления, которым обладал бы компонент, подчиняющийся данному уравнению состояния при температуре и мольном объеме смеси. [8]
NI) равна величине давления, которым обладал бы г - й компонент, подчиняющийся данному уравнению состояния при температуре Т и мольном объеме смеси v; NL - мольная доля данного компонента. [9]
Таким образом, для перевода свойства, аддитивного при выражении состава в объемных долях, в мольно-аддитивную модификацию необходимо свойство смеси умножить на значение мольного объема смеси, а значения свойств компонентов - на значения их мольных объемов. [10]
V, N) равна величине давления, которым обладал бы 1 - й компонент, подчиняющийся данному уравнению состояния при температуре Т и мольном объеме смеси V; Л /; - - мольная доля данного компонента. [11]
Аммиак, согласно условию задачи, занимает 34 об. % и, следовательно, в этом объеме его содержится 0 34 моля, что составляет 17 0 34 г. Рассуждая аналогично, прийдем к выводу, что масса водорода в смеси, заключенной в мольном объеме, составляет 2Х г, а масса азота - 28 ( 1 - 0 34 - X) г. Таким образом, в мольном объеме смеси заключено [ 17 0 34 - f 2X 28 ( 1 - 0 34 - X) ] г газа и 42 5 мае. [12]
 |
Зависимость коэффициента сжимаемости z метана от приведенной температуры ( Пример. [13] |
Проводим изохоры по заданным мольным объемам смеси. [14]
 |
Разделение фаз.| Разделение фаз. [15] |
Страницы: 1 2