Парциальный мольный объем
Cтраница 2
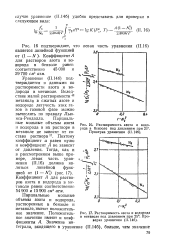 |
Растворимость азота и водорода в бензоле под давлением при 25. Проверка уравнения ( II. 146.| Растворимость азота и водорода в метаноле под давлением при 25. Проверка уравнения ( II. 146. [16] |
Парциальные мольные объемы азота и водорода, растворенных в бензоле и метаноле, имеют положительное значение. Положительное значение имеют и коэффициенты А. [17]
Парциальные мольные объемы ацетона и хлороформа в растворе с мольной долей хлороформа 0.469 3 равны 74.166 и 80.235 см3 - моль -, соответственно. [18]
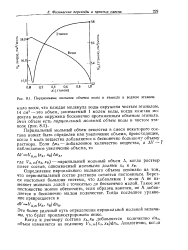 |
Парциальные мольные объемы воды и этанола в водном этаноле. [19] |
Парциальный мольный объем вещества в смеси некоторого состава может быть определен как увеличение объема, происходящее, когда 1 моль вещества добавляется к бесконечно большому объему раствора. [20]
Парциальный мольный объем надкритических компонентов, строго говоря, может изменяться с изменением состава жидкой фазы. [21]
Парциальный мольный объем растворенного неона определялся графически - методом засечек [4] ( фиг. Рассчитанные значения парциального мольного объема неона в зависимости от давления приведены ниже. [22]
Парциальный мольный объем псевдооднокомпонентного растворителя тоже должен совпадать с критическим мольным объемом азеотропной смеси. [23]
Определите парциальные мольные объемы обоих компонентов при этих составах и изобразите результат графически. [24]
Определить парциальный мольный объем азотнокислого, аммония в водном растворе, если парциальный мольный объем воды равен 17 98 см3, объем раствора 93 87 см3, концентрация 16 г NH4NO3 в 100 г раствора. [25]
Определить парциальный мольный объем спирта, если плотность 60 % - ного водного раствора метилового спирта при 293 К равна 0 8946 г / см3, парциальный мольный объем воды в этом растворе 16 8 см3 / моль. [26]
Определить парциальный мольный объем азотнокислого аммония в водном растворе, если парциальный мольный объем воды составляет 17 98 см3, объем раствора 86 87 см3, концентрация 35 г NH4NO3 в 100 г раствора. [27]
Очень часто парциальные мольные объемы сравнительно неполярных веществ в водном растворе значительно меньше, чем объемы чистых веществ; широко известным примером служит уменьшение объема при смешивании спирта с водой. Это можно объяснить рыхлостью структуры жидкой воды, из-за чего слабо взаимодействующие молекулы могут легко проникать в пустоты при сравнительно малом увеличении общего объема. Большой мольный объем воды при полном использовании всех возможных водородных связей несомненно проявляется в низкой плотности льда и позволяет приемлемо объяснить, что вода обладает максимальной плотностью при температуре на несколько градусов выше температуры плавления. Увеличение объема при понижении температуры от температуры максимальной плотности до температуры плавления связано с увеличением числа водородных связей и структурированием воды при приближении к состоянию с максимальным числом водородных связей. Не будем вникать в дискуссию по поводу того, можно ли точно описать жидкую воду как двухструктурную систему, состоящую из областей структурированной воды с низкой плотностью и областей с высокой плотностью, где молекулы воды неупорядочены. Отметим лишь, что детали этой дискуссии не влияют на пригодность качественной концепции, заключающейся в том, что возрастание структурированности или числа линейных водородных связей связано с увеличением количества воды, имеющей низкую плотность. [28]
Зависимость парциального мольного объема от дисперсности частиц не позволяет исключить из рассмотрения в термодинамике строение поверхностного слоя даже - при определении парциальных величин для термодинамических функций, определяемых с помощью метода избытков. [29]
Значения парциальных мольных объемов его vt в различных растворителях могут оказаться разными, что приведет к различному росту активностей растворенного вещества в обеих фазах. Но эти активности, согласно закону распределения, должны быть при равновесии всегда пропорциональны друг другу; следовательно, при высоком давлении будет происходить переход вещества из одной фазы в другую. [30]
Страницы: 1 2 3 4