Парциальный мольный объем - растворенное вещество
Cтраница 2
 |
Приближенные оценки мольного объема и коэффициента теплового расширения критического комплекса а для реакции между йодистым этилом и пиридином. [16] |
Мольные объемы были определены лишь в немногих случаях, причем, по всей вероятности, парциальные мольные объемы растворенного вещества в растворе и в чистом состоянии не совпадают. [17]
Конечно, и в отсутствие этих сольватационных эффектов природа растворителя влияет на изменение константы скорости реакции с повышением давления, так как в результате действия межмолекулярных ( ван-дер-ваальсовых) сил, а также особенностей структуры растворителей парциальные мольные объемы растворенных веществ различаются в разных растворителях, хотя и не на очень значительную величину. Это видно, в частности, из данных табл. 24 ( стр. [18]
 |
Приближенные оценки мольного объема и коэффициента. теплового расширения критического комплекса а для реакции между йодистым этилом и пиридином. [19] |
Точно так же, как нельзя оценить энергию активированного комплекса ( неточно называемого переходным состоянием), не зная парциальных мольных энергий растворенного вещества в основном состоянии, нельзя установить и объем критического комплекса, если не известны парциальные мольные объемы растворенных веществ в основном состоянии. Мольные объемы были определены лишь в немногих случаях, причем, по всей вероятности, парциальные мольные объемы растворенного вещества в растворе и в чистом состоянии не совпадают. [20]
Критические бесконечно разбавленные растворы на пути Р PIK, Т TljK имеют много общего с обычными бесконечно разбавленными растворами, но во многом и отличаются от них. Но парциальный мольный объем растворенного вещества в критическом бесконечно разбавленном растворе, в отличие от парциального мольного объема растворенного вещества в обычном бесконечно разбавленном растворе, стремится к бесконечности. Есть и другие различия, одно описано ниже. [21]
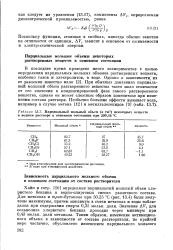 |
Парциальный мольный объем ( в см3 некоторых веществ в водном растворе в основном состоянии при 290 16 С. [22] |
В последнее время проведено много экспериментов е целью определения парциальных - мольных объемов растворенных веществ, особенно газов и электролитов, в воде. При обычных давлениях парциальный мольный объем растворенного вещества часто мало отличается от его значения в конденсированной фазе самого растворенного вещества, однако он может сложным образом изменяться при изменении состава раствора. [23]
В последнее время проведено много экспериментов с целью определения парциальных мольных объемов растворенных веществ, особенно газов и электролитов, в воде. При обычных давлениях парциальный мольный объем растворенного вещества часто мало отличается от его значения в конденсированной фазе самого растворенного вещества, однако он может сложным образом изменяться при изменении состава раствора. [24]
Найдены значения парциального мольного объема нафталина в его бесконечно разбавленном растворе в этилене. Показано, что в соответствии с теорией парциальный мольный объем растворенного вещества при его мольной доле, стремящейся к нулю, приближается к бесконечности. [25]
В самих этих критических точках ( Л 2 - - 0) парциальный мольный объем растворенного вещества стремится, как известно, к бесконечности. [26]
Точно так же, как нельзя оценить энергию активированного комплекса ( неточно называемого переходным состоянием), не зная парциальных мольных энергий растворенного вещества в основном состоянии, нельзя установить и объем критического комплекса, если не известны парциальные мольные объемы растворенных веществ в основном состоянии. Мольные объемы были определены лишь в немногих случаях, причем, по всей вероятности, парциальные мольные объемы растворенного вещества в растворе и в чистом состоянии не совпадают. [27]
Критические бесконечно разбавленные растворы на пути Р PIK, Т TljK имеют много общего с обычными бесконечно разбавленными растворами, но во многом и отличаются от них. Но парциальный мольный объем растворенного вещества в критическом бесконечно разбавленном растворе, в отличие от парциального мольного объема растворенного вещества в обычном бесконечно разбавленном растворе, стремится к бесконечности. Есть и другие различия, одно описано ниже. [28]
 |
Парциальные мольные объемы хлористого бензила в водно-спиртовых растворах при 50 25. С. [29] |
Тот факт, что кажущаяся энергия активации есть мера разности между средней энергией активных молекул и средней энергией всех молекул вообще, справедлив только для случая, когда вероятность распада активных молекул не зависит от температуры. Теперь мы знаем, что это условие выполняется редко. Точно так же кажущийся объемный эффект активации есть мера разности между парциальным мольным объемом активированного комплекса и суммой парциальных мольных объемов растворенных веществ в основном состоянии только тогда, когда вероятность распада комплекса не зависит от давления. [30]
Страницы: 1 2 3