Бикарбонат - магний
Cтраница 1
Бикарбонат магния, Mg ( HC03) 2, представляет собой твердое вещество белого цвета, очень неустойчивое. [1]
Бикарбонаты магния могут выпадать в порах грунта в виде хлопьев Mg ( ОН) 2 лишь при рН, равном 10 5 - И, 0 и выше, что имеет место в редких случаях. [2]
Разложение бикарбоната магния протекает по аналогичному уравнению. Образующиеся карбонаты кальция и магния нерастворимы в воде и выпадают в осадок, причем жесткость воды, обусловленная бикарбонатами указанных металлов, устраняется. Кипячением некарбонатная жесткость воды не устраняется. [3]
Разложение бикарбоната магния протекает по аналогичному уравнению. Образующиеся карбонаты кальция и магния нерастворимы в воде и выпадают в осадок, причем жесткость воды, обусловленная бикарбонатами указанных металлов, устраняется. Путем кипячения некарбонатная жесткость воды не устраняется. [4]
Декарбонизация раствора бикарбоната магния с получением основной соли ускоряется при продувке через раствор воздуха. Однако этот воздух значительно снижает концентрацию выделяющейся в этом процессе двуокиси углерода, что затрудняет ее возврат на карбонизацию. Поэтому вначале разложение раствора ведут только при механическом перемешивании с использованием выделяющегося газа. После снижения концентрации MgO до 4 г / л через раствор начинают продувать воздух, причем выделяющийся газ выбрасывают в атмосферу. [5]
В кристаллическом состоянии бикарбонат магния был получен при 0 С под давлением СОа в 18 ат. [6]
В кристаллическом состоянии бикарбонат магния был получен при 0 С под давлением СО2 в 18 ат. [7]
 |
Термоумягчитель системы Копьева. [8] |
При наличии в воде бикарбоната магния процесс перехода его в осадок происходит следующим образом. [9]
Бикарбонат кальция наряду с бикарбонатом магния обусловливает временную жесткость воды. Жесткость воды выражается в градусах ( старая единица) и в миллиграмм-эквивалентах на 1 л воды ( новая единица) ( см. примечание стр. [10]
Бикарбонат кальция наряду с бикарбонатом магния обусловливает временную жесткость воды. [11]
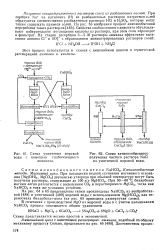 |
Схема умягчения морской.| Схема катионообменного. [12] |
При 50 - 60 С бикарбонат магния легко разлагается с выделением СО2 и нерастворимого MgCO3, тогда как NaHCO3 в этих же условиях устойчив. [13]
Как относятся к нагреванию карбонат и бикарбонат магния. [14]
После достижения максимального пересыщения раствора по бикарбонату магния из него начинают кристаллизоваться гидрокар-бонатные соединения магния, в частности, пента или тригидрокарбо-нат магния. [15]
Страницы: 1 2 3 4