Окисление - ион - двухвалентное железо
Cтраница 1
Окисление ионов двухвалентного железа протекает количественно в сернокислой среде. [1]
После окисления ионов двухвалентного железа соотношение [ Fe3 ]: [ Fe2 ] резко изменяется и в этот момент наблюдается большой скачок потенциала. [2]
Реакция окисления иона двухвалентного железа кислородом, схема которой приведена на стр. [3]
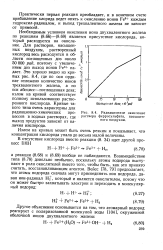 |
Радиационное окисление раствора ферросульфата, насыщенного воздухом. [4] |
Необходимым условием окисления иона двухвалентного железа по реакциям (8.66) - (8.69) является присутствие кислорода, который расходуется на окисление. Для растворов, насыщенных воздухом, растворенный кислород весь расходуется в области поглощенных доз около 50 000 рад, поэтому с увеличением доз выход ионов Fe3 падает. Это хорошо видно, из кривых рис. 8.4, где по оси ординат отложено количество ионов трехвалентного железа, а по оси абсцисс-поглощенная доза; излом на кривой соответствует полному использованию растворенного кислорода. [5]
Скорость всего процесса окисления ионов двухвалентного железа в целом определяется реакцией ( I), так как реакция ( II), протекающая по радикальному механизму, является более быстрой. [6]
Хлорид натрия добавляют как ингибитор окисления ионов двухвалентного железа органическими примесями [32], его можно не применять, если реагенты и вода хорошо очищены. Очень важным фактором является чистота воды любых облучаемых растворов. Дистиллированная вода обычно очищается повторной дистилляцией из щелочного раствора перманганата и затем из кислого раствора бихромата; это уменьшает количество органических примесей. Такая вода называется трижды перегнанной. Однако и такой дистилляции недостаточно для полного удаления примесей. Деионизованная вода не применяется в радиационно-химических исследованиях. [7]
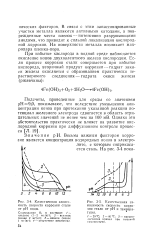 |
Качественная зависимость скорости коррозии стали от рН воды.| Качественная зависимость скорости коррозии стали от рН и температуры. [8] |
При избытке кислорода в водной среде наблюдается окисление ионов двухвалентного железа кислородом. [9]
VIII упоминалось о том, что в цехе выщелачивания, в кислой ветви, для окисления ионов двухвалентного железа в раствор добавляют двуокись марганца. В результате реакции VII в растворе вакапливаются ионы двухвалентного марганца. [10]
В зимнее время содержание кислорода в воде составляло примерно 0 8 - 1 мг / л, что было совершенно недостаточным для окисления ионов двухвалентного железа и перевода его в трехвалентное. [11]
При добавлении к раствору, содержащему ферри - и ферро-ионы, раствора, содержащего цери - и церо-ионы, реакция будет протекать в сторону окисления ионов двухвалентного железа и восстановления ионов четырехвалентного церия; в состоянии равновесия железо будет практически полностью окислено до ферри-ионов, а церий восстановлен до церо-ионов. [12]
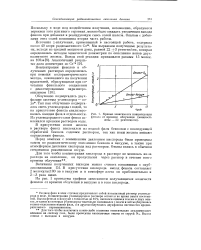 |
Кривые зависимости концентрации. [13] |
Мы выражаем полученные результаты, исходя из средней мощности дозы, равной 22 3 рентген / сек, которая определялась методом химической дозиметрии по окислению ионов двухвалентного железа. [14]
 |
Зависимость выхода окисления двухвалентного железа от его концентрации, по данным Дейнтона и Саттона. [15] |
Страницы: 1 2