Окисление - уксусный альдегид
Cтраница 1
Окисление уксусного альдегида может происходить как в жидкой, так и в газовой фазе. При окислении в газовой фазе выделяется большое количество теплоты, и часть уксусного альдегида может сгореть. [1]
Окисление уксусного альдегида проводится в более мягких условиях, при меньшей кислотности среды. Эти авторы показали, что увеличение числа атомов хлора в молекуле этана повышает устойчивость ее к окислению бихроматом. Трихлоруксусная кислота в условиях окисления хлоралгидрата не окисляется, что было подтверждено экспериментально. [2]
Окисление уксусного альдегида проходит довольно медленно, и в промышленности неокисленный альдегид направляют на повторное окисление. Осуществить окисление уксусного альдегида в лабораторных условиях по циркуляционной схеме довольно трудно. [3]
Окисление уксусного альдегида является важным промышленным спосо бом производства уксусной кислоты. [4]
Окислением уксусного альдегида кислородом воздуха в присутствии катализаторов ( солей Мп) приготовляют для технических целей значительные количества уксусной кислоты. [5]
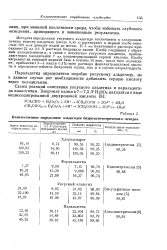
Процесс окисления уксусного альдегида в уксусную кислоту идет со значительным выделением тепла. Однако большая поверхность змеевика ( 175 м2) позволяет поддерживать температуру в реакционной массе в пределах 60 - 70 С. Верхняя ( расширенная) царга служит брызгоуловителем. Все части колонны и змеевики, соприкасающиеся со средой, изготовлены из кислотостойкой стали. В нижнюю часть колонны подается уксусный альдегид с раствором катализатора и кислород. Благодаря большому количеству змеевиков в колонне образуется своеобразная насадка, обеспечивающая хороший контакт между жидкостью и кислородом. Для разбавления парогазовой фазы в верхнюю часть колонны подается азот. [6]
Колонна окисления уксусного альдегида: / - корпус; 2-охлаждающие змеевики; 3 - брызгоуловитель. [7]
 |
Количественное определение альдегидов бихроматометрическим методом. [8] |
Схемы реакций окисления уксусного альдегида и паральдеги-да аналогичны. [9]
Современные процессы окисления уксусного альдегида позволяют одновременно получать уксусную кислоту и уксусный ангидрид. [10]
Получают пероксиуксусную кислоту окислением уксусного альдегида кислородом. [11]
В промышленности его получают окислением уксусного альдегида кислородом воздуха на медно-кобаль-товом катализаторе. [12]
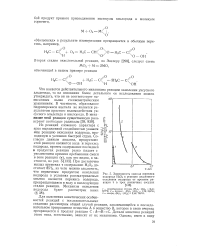 |
Зависимость выхода перекиси водорода Н2О2 в реакции медленного окисления водорода от времени реакции t в трех различных сосудах. [13] |
Что касается действительного механизма реакции окисления уксусного альдегида, то на основании более детального ее исследования можно утверждать, что он не соответствует написанным выше стехиометрическим уравнениям. В частности, образование гидроперекиси ацетила не является результатом простого взаимодействия уксусного альдегида и кислорода. [14]
В ряде работ, посншцелпых окислению уксусного альдегида, отмечается, что в продуктах окисления обнаруживаются перекиси, формальдегид, метиловый спирт и кислоты: уксусная и муравьиная. Но подлежит сомнению, что состав конденсата определялся эффективностью закалки реакции. [15]
Страницы: 1 2 3 4