Бинафтил
Cтраница 1
Бинафтил также возможно разделить на антиподы. Впервые он был получен в оптически активной форме дезаминирова-нием ( - ( -) - 4 4 -диамино - 1 Г - бинафтила. [1]
Бинафтил, 2 2 -дигидрокси - 414, 421, 424 Бис ( 2-ацетоксиэтиловый) эфир 410 Бис ( 2-бромэтиловый) эфир 410 Бис ( трифенилметил) пероксид 470 Бисфенол А, тетригидрокси - 275 Бис ( хлорметиловый) эфир 348 Бифенил. [2]
Дигидрокси-1 Г - бинафтил при нагревании в нитробензоле в присутствии оксида марганца ( IV) превращается в диоксид бинафтилена. [3]
Диамино-2 2 -бинафтил 289 2 2 - Диамяно-1 Г - бинафтил 289 4 4 - Диамино-1 Г - бинафтил 289 2 2 - Диаминобифенил 288, 777 4 4 - Диаминобифенил см. Бензидин Диаминогеновая кислота 185, 303 Диаминодиарилметановые производные 711, 713 ел. [4]
Диамино-2 2 -бннафтил 289 2 2 - Диамино-1 1 -бинафтил 289 4 4 - Диамино-1 Г - бинафтил 289 2 2 - Диаминобифенил 288, 777 4 4 - Диаминобифенил см. Бензидин Диаминогеновая кислота 185, 303 Диаминодиари листа новые производные 711, 713 ел. [5]
Диамино-2 2 -бинафтил 289 2 2 - Диамяно-1 Г - бинафтил 289 4 4 - Диамино-1 Г - бинафтил 289 2 2 - Диаминобифенил 288, 777 4 4 - Диаминобифенил см. Бензидин Диаминогеновая кислота 185, 303 Диаминодиарилметановые производные 711, 713 ел. [6]
Гидразопроизводные нафталина по Л. Г. Кролик и В. О. Лукашевичу перегруппировываются в диаминопроизводные бинафтила и в отсутствие кислот. Так, Ы - гидразонафталин при нагревании в спиртовой среде образует 4 4 -ди-амкно - 1 Г - бинафтил и 1Гдиамино - 2 2 -бинафтил. Аналогично 2 2 -гидразонафта-лин при нагревании в бензоле образует 2 2 -диамино - 1 Г - бинафтил. [7]
Чаще всего копланарность молекулы нарушается вследствие свободного вращения отдельных частей молекулы вокруг простой С - С-связи. Например, в молекуле бинафтила возможен поворот двух нафталиновых ядер вокруг а-связи С - С, что нарушает сопряжение и-электронов ароматических ядер, поэтому бинафтил - бесцветное соединение. [8]
Оптическая активность получаемого полимера вызывается исключительно спиральностью - пропеллерным расположением фенильных ядер. Особый интерес представляет применение этого адсорбента для расщепления углеводородов - 2-фенил-бутана ( ОЧ 2 %), гексагелицена ( ОЧ 57 %), а также бинафтилов с аксиальной хиральностью, основания Трегера, амидов и эфиров цикло-гександикарбоновых кислот. [9]
Наличие изотопного эффекта атомов азота и атома углерода в пара-положении указывает, что о-бензидиновая перегруппировка 2 2 / - гидразонафталина в 2 2 -диамино - 1 1л - бинафтил также протекает как согласованная, путем [3,3] - сигматропного сдвига. [10]
Гидразопроизводные нафталина по Л. Г. Кролик и В. О. Лукашевичу перегруппировываются в диаминопроизводные бинафтила и в отсутствие кислот. Так, 1 Г - гидразонафталин при нагревании в спиртовой среде образует 4 4 -ди-амино - 1 1 -бинафтил и 1Гдиамино - 2 2 -бинафтил. Аналогично 2 2 -гидразонафта-лин при нагревании в бензоле образует 2 2 -диамино - 1 Г - бинафтил. [11]
Гидразопроизводные нафталина по Л. Г. Кролик и В. О. Лукашевичу перегруппировываются в диаминопроизводные бинафтила и в отсутствие кислот. Так, Ы - гидразонафталин при нагревании в спиртовой среде образует 4 4 -ди-амкно - 1 Г - бинафтил и 1Гдиамино - 2 2 -бинафтил. Аналогично 2 2 -гидразонафта-лин при нагревании в бензоле образует 2 2 -диамино - 1 Г - бинафтил. [12]
Выходы низки, и реакция редко оказывается полезной с синтетической точки зрения. Для проведения реакции необходимо применять высокие температуры и сильные кислоты в качестве катализаторов, поэтому реакция не пригодна для субстратов, которые разрушаются в этих условиях. Поскольку роль этой реакции возрастает при переходе к большим конденсированным системам, обычные реакции по Фриделю - Крафтсу ( реакция 11 - 13) с такими системами редки. Например, в услових проведения реакций Фриделя - Крафтса нафталин дает бинафтил. [13]
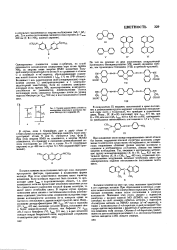 |
Уровни энергии НМО и НСМО и электронные переходы в молекулах гид-рола Михлера ( а н аурамина ( б. [14] |
При этом существенное значение имеет характер искажения. В первом случае причина повышения цвета связана с частичным или полным разобщением отдельных участков цепи сопряжения вследствие нарушения когшанарности молекулы из-за поворота одних ее частей по отношению к другим вокруг простой связи. Чп с 432 нм), имеющие плоскую форму, поглощают свет в более длинноволновой области, чем бифенил ( V; Х, 251 5 нм) и бинафтил ( VI; с 291 нм), у к-рых возможен поворот вокруг биарильной связи, нарушающий сопряжение 71-электронов двух ароматич. [15]
Страницы: 1