Гетерогенное окисление - окись - азот
Cтраница 1
Гетерогенное окисление окиси азота концентрированной азотной кислотой связано с растворением N0 в азотной кислоте, взаимодействием с нею окиси азота, а также с образованием азотистой кислоты, ее разложением на NO2 и Н2О и десорбцией двуокиси азота при понижении концентрации азотной кислоты и повышении температуры. [1]
Гетерогенное окисление окиси азота концентрированной азотной кислотой связано с растворением NO в азотной кислоте, взаимодействием с нею окиси азота, а также с образованием азотистой кислоты, ее разложением на NO2 и Н2О и десорбцией двуокиси азота при понижении концентрации азотной кислоты и повышении температуры. [2]
Продолжительность процесса гетерогенного окисления окиси азота исчисляется секундами, однако на его осуществление расходуется часть концентрированной азотной кислоты. [3]
Продолжительность процесса гетерогенного окисления окиси азота исчисляется секундами, однако на его осуществление расходуется часть концентрированной азотной кислоты. Несмотря на некоторое снижение скорости окисления NO концентрированной азотной кислотой с понижением температуры, целесообразно вести процесс именно при пониженной температуре газа, так как при этом уменьшается количество водяных паров, уносимых нитрозными газами. [4]
В присутствии этих катализаторов скорость реакции гетерогенного окисления окиси азота увеличивается в 1 5 - 2 5 раза. [5]
Если при гомогенной реакции присутствие небольших количеств паров воды увеличивает константу скорости примерно на 10 %, то при гетерогенном окислении окиси азота в присутствии паров воды скорость реакции быстро падает вследствие отравления катализатора. [6]
Если при гомогенной реакции в присутствии небольшого количества паров воды константа скорости увеличивается примерно на 10 %, то при гетерогенном окислении окиси азота в присутствии паров воды скорость реакции быстро уменьшается вследствие отравления катализатора. По данным Г. К. Борескова, в присутствии активированного угля порядок реакции снижается до 2 5, и она тормозится образующейся двуокисью азота. [7]
Если при гомогенной реакции в присутствии небольшого количества паров воды константа скорости увеличивается примерно на 10 %, то при гетерогенном окислении окиси азота в присутствии паров воды скорость реакции быстро уменьшается вследствие отравления катализатора. [8]
При регенерации и выделении окиси азота из раствора ее концентрация на границе раздела фаз повышается, что создает благоприятные условия для ускорения гетерогенного окисления окиси азота. [10]
Если же локрыть стенки сосуда парафином, скорость реакции заметно замедляется. Это указывает на возможность гетерогенного окисления окиси азота. [11]
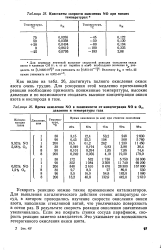 |
Константы скорости окисления NO при низких температурах.| Время окисления NO в зависимости от концентрации NO и О2, давления и температуры газа. [12] |
В результате скорость реакции окисления значительно увеличивалась. Если же покрыть стенки сосуда парафином, скорость реакции заметно замедляется. Это указывает на возможность гетерогенного окисления окиси азота. [13]
Ускорение реакции может быть достигнуто также применением катализаторов. В результате оказалось, что скорость реакции окисления значительно увеличивалась. Если же покрыть стенки сосуда парафином, то скорость реакции заметно замедляется. Это указывает на возможность и гетерогенного окисления окиси азота. [14]
Страницы: 1
