Низкотемпературное окисление - углеводород
Cтраница 1
Низкотемпературное окисление углеводородов трудно регулировать. Этот процесс представляет собой свободнорадикальную цепную реакцию и первые продукты ее - гидроперекиси. Реакцию иногда используют для получения тпрет-гидроперекисей. [1]
Низкотемпературное окисление углеводородов трудно регулировать. Этот процесс представляет собой свободнорадикальную цепную реакцию и первые продукты ее - гидроперекиси. Реакцию иногда используют для получения ягретп-гидронерекисей. [2]
Жидкофазное низкотемпературное окисление углеводородов является весьма перспективным методом их переработки. [3]
Неполное низкотемпературное окисление углеводородов природных и попутных газов является одним из наиболее перспективных методом получения продуктов органического синтеза, так как дает возможность превращать дешевое сырье в ценные кислородсодсржащие соединения - спирты, альдегиды, кетопы. [4]
Неполное низкотемпературное окисление углеводородов природных и попутных газов является одним из наиболее перспективных методов получения продуктов органического синтеза, так как дает возможность превращать дешевое сырье в ценные кислородсодержащие соединения - спирты, альдегиды, кетоны. [5]
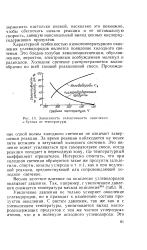 |
Зависимость селективности окисления н-бутана от температуры. [6] |
Характерной особенностью низкотемпературного окисления углеводородов является появление холодного свечения. Это бледно-голубая хемилюминесценция, обусловленная, вероятно, электронным возбуждением молекул и радикалов. Холодное свечение распространяется волнообразно по всей газовой реакционной смеси. [7]
В случае низкотемпературного окисления углеводородов образуются такие кислородные соединения, как и двуокись углерода; при высокотемпературном окислении получаются алкены и более низкомолекулярные алканы, что доказывает протекание реакций расщепления ( крекинга) и дегидрирования. Относительные выходы продуктов окисления бутана в зависимости от температуры показаны на рисунке. Максимальный выход кислородных соединений наблюдается при минимальной температуре, при которой может протекать окисление; дальнейшее повышение температуры приводит к неуклонному снижению выхода кислородных соединений. При дальнейшем повышении температуры появляются более низкомолекулярные алкены и алканы в прогрессивно возрастающих количествах, в то время как образование кислородных соединений и некрекированных алкенов снижается. [8]
Характерным явлением при низкотемпературном окислении углеводородов следует считать возникновение бледно-голубой люминесценции, или холодного пламени, сопровождающего быстрое окисление. [9]
Так, при низкотемпературном окислении углеводородов и присоединении С12 к С2Н4 исходные вещества расходуются в обеих стадиях продолжения цепи, а продукты образуются только во второй стадии. В реакциях распада СН3СНО и С2Н8 в обеих стадиях образуются продукты реакции, но лишь в первой расходуется исходное вещество. [10]
Характерным явлением при низкотемпературном окислении углеводородов следует считать возникновение бледно-голубой люминесценции, или холодного пламени, сопровождающего быстрое окисление. [11]
Так, в случае низкотемпературного окисления углеводородов и в случае присоединения С12 к С2Н4 исходные вещества расходуются в обеих реакциях продолжения цепи, а продукты реакции образуются только во второй реакции. [12]
Так, в случае низкотемпературного окисления углеводородов и присоединения С12 к С2Н4 исходите вещества расходуются в обеих реакциях продолжения цепи, а продукты образуются только во второй реакции. [13]
Возникновение холодного пламени при низкотемпературном окислении углеводородов объясняется развитием цепного радикального процесса за счет первичной термической диссоциации углеводородов. [14]
А, отмечавшееся многими исследователями при низкотемпературном окислении углеводородов. [15]
Страницы: 1 2