Окись - литий
Cтраница 1
Окись лития смешивают с окисью кальция и восстанавливают алюминием или феррокремнием. Смесь брикетируют и нагревают в трубчатой вакуум-печи ( вакуум 10 - 6 мм рт. ст.) в течение 15 час. [1]
Окись лития [ Li2O ] устойчива; перекись лития [ Li2O2 ] разлагается с выделением части своего кислорода уже при 160; надокись [ LiO2 ] очень неустойчива, и первые сведения о ней получены совсем недавно. [2]
Окись лития представляет собой частично спекшуюся массу, которую измельчают в фарфоровой ступке. [3]
Окись лития Li2O заметно улучшает плавкость и смачивающую способность покрытий при сравнительно небольшом ее содержании в эмали. Окись лития применяют для приготовления стеклокристаллических ( ситалловых) покрытий с низким коэффициентом теплового расширения. Ее вводят в шихту, используя углекислый литий. [4]
Окись лития получается при сжигании металла в отсутств. [5]
Окись лития гидратируется сравнительно медленно. Напротив, окислы остальных щелочных металлов реагируют с золой весьма энергично. Взаимодействие протекает по схеме Э2О НгО 2ЭОН и сопровождается большим выделением тепла. Непосредственного применения окислы щелочных металлов пока не находят. [6]
Окись лития Li2O заметно улучшает плавкость и смачивающую способность покрытий при сравнительно небольшом ее содержании в эмали. Окись лития применяют для приготовления стеклокристаллических ( ситалловых) покрытий с низким коэффициентом теплового расширения. Ее вводят в шихту, используя углекислый литий. [7]
Окись лития, согласно исследованию Н. В. Соломина [43], при замещении ею окиси натрия понижает коэффициент термического расширения стекла, что может быть использовано для изготовления термически стойкой глазури. [8]
Окись лития корродирует большинство даже коррозионно-устойчивых материалов, легко разрушает многие металлы и взаимодействует со многими окислами. Ниже 1000 устойчивы против Li2O никель, золото и платина. [9]
Окись лития не может быть восстановлена водородом, углеродом или окисью углерода. [10]
Окись лития Li2O представляет собой устойчивое соединение пития и кислорода, однако она очень легко реагирует с водой, двуокисью углерода и многими тугоплавкими соединениями. [11]
Окись лития получают прокаливанием перекристаллизованного карбоната лития ( несколько граммов) в платиновой или железной лодочке, которую помещают в фарфоровую трубку и постепенно нагревают в трубчатой лечи в течение 0 5 - 1 ч ниже температуры плавления карбоната, примерно до 650 С, а затем температуру постепенно повышают до 800 С или несколько выше. [12]
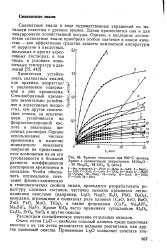 |
Кривые окисления при 800 С железа Армко с силикатными покрытиями 16Na2O 20 МетО 64 SiO2, % ( мол.. [13] |
Окись лития Li2O - наиболее сильный плавень среди щелочных окислов и не так легко разлагается водными реагентами, как другие щелочные окислы. [14]
Окись лития Li2O плавится при температуре выше 1700 С, а окись натрия Na2O - при 920 С. Окиси других щелочных металлов, не достигая температуры плавления, разлагаются. [15]
Страницы: 1 2 3 4