Окись - магний
Cтраница 3
Окись магния, силикаты магния ( например, Florisil), карбонат кальция, а также полистирол и полиамиды имеют свои области применения в адсорбционной хроматографии, главным образом в неполярных растворителях, но в процессах очистки и фракционирования белков и НК они практически не используются. [31]
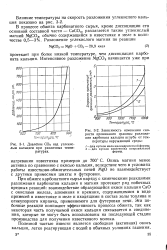 |
Давление СО2 над углекислым кальцием при различных температурах.| Зависимость изменения скорости проникания границы разложения карбоната кальция вглубь от температуры окружающей среды. [32] |
Окись магния менее активна по сравнению с окисью кальция, вследствие чего в условиях работы известково-обжигательных печей MgO не взаимодействует с другими примесями шихты и футеровки. [33]
Окись магния смешивают с углем и брикетируют. В результате восстановления ( MgO - j - С Mg - р СО) металл получается в парообразном виде. Дальнейшее охлаждение смеси проводят в холодильниках. MgO и углерода от смеси газов производят с помощью мешочных фильтров. MgO и С, используют как наполнитель резины. [34]
Окись магния безводная: чистую окись магния прокаливают при температуре около 700 С и просеивают через сито 0 5 мм. Хранят в закрытой банке. [35]
Окись магния, прокаленная при 600 - 700 С. [36]
Окись магния частично нейтрализует фосфорную кислоту, образуя растворимые фосфаты магния. Газообразная двуокись углерода способствует образованию пены, нарушающей разложение фосфата. [37]
Окись магния ( жженая магнезия, magnesia usta) применяется как легкое слабительное и для нейтрализации соляной кислоты при повышенной кислотности. Употребляется также ( аналогично животному углю) как поглотитель различных газообразных веществ. [38]
Окись магния получают прокаливанием карбонатов или гндрокарбонатов в фарфоровом тигле в муфельной печи. Разложение карбоната ( MgCO3 MgO CO2) начинается при 300 С, а заканчивается при температуре красного каления. [39]
Окись магния вызывает образование в карбидной печи тугоплавких шлаков. Карбид кальция в этом случае получается также тугоплавким, что затрудняет выпуск его из печи. Кроме того, окись магния в электропечи разлагается, на что также расходуется электроэнергия. Окись алюминия также способствует образованию тугоплавких окислов. [40]
Окись магния восстанавливается до парообразного магния, вызывая дополнительный расход кокса и электроэнергии. Содержание MgO в извести не должно превышать 1 вес. [41]
Окись магния получают прокаливанием карбонатов ( основных или средних) в фарфоровом тигле и в муфельной печи. [42]
Окись магния получают из рассолов путем осаждения известью. Для получения ее пригодны даже такие разбавленные рассолы, как морская вода, в которой содержится только 0 14 % магния. Однако для получения окиси магния удобнее использовать обез-бромленные рассолы, так как рассолы после обработки известью имеют высокую щелочность и поэтому из них уже нецелесообразно получать бром. [43]
 |
Кривая нагревания Mg ( OH2. [44] |
Окись магния, будучи в аморфном состоянии, при действии воды гидратируется, превращаясь при этом в гидроокись магния. Последняя реагирует с аморфной кремнекислотой с образованием гидравлического вяжущего вещества - гидросиликата магния. [45]
Страницы: 1 2 3 4