Красная окись - железо
Cтраница 3
Оттенок красной окиси железа зависит преимущественно от температуры прокаливания, но определенное влияние оказывает также и исходное соединение железа. [31]
Оттенок красной окиси железа, в зависимости от условий ее получения, может колебаться от оранжево-красного до синеватого и даже фиолетово-красного. [32]
Свойства красной окиси железа находятся в зависимости от ее оттенка: уд. [33]
 |
Кривая обезвоживания семивод - ся и теряется при промывке. [34] |
При получении красной окиси железа прокаливанием кристаллического железного купороса FeSC4 7Н2О обычно получается пигмент, содержащий большое количество крупных спекшихся частиц. Наличие таких частиц объясняется растворением FeSO4 - 7H2O при нагревании в кристаллизационной воде, которая быстро испаряется при высокой температуре, оставляя железный купорос в виде твердой спекшейся массы. Последняя и служит причиной появления в пигменте спекшихся частиц. Предупредить их образование можно предварительным обезвоживанием железного купороса, которое может происходить даже при комнатной температуре, хотя и очень медленно. Повышение температуры сильно ускоряет процесс: при 60 скорость обезвоживания становится достаточно заметной, а при Ю0 шесть молекул воды удаляются очень быстро. [35]
Для получения красной окиси железа применяют преимущественно сернокислую соль закиси железа ( железный купорос), значительно реже - сернокислую соль окиси железа. Железный купорос иногда прокаливают в смеси с мелом. [36]
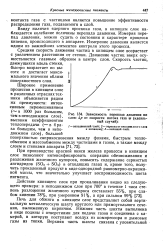 |
Зависимость перепада давления по слою Др от скорости потока газа w ( идеальный случай. [37] |
При производстве красной окиси железа процессы в кипящем слое позволяют интенсифицировать операции обезвоживания и разложения железного купороса, повысить содержание сернистых ангидридов ( SO2 SO3) в отходящих газах и, кроме того, получить прокаленный продукт в виде однородной равномерно-окрашенной массы, что значительно улучшает воспроизводимость цвета пигмента. [38]
 |
Электронные микрофотографии красной окиси железа с подтенением ( X 90000. [39] |
Диаметр частиц красной окиси железа ( рис. VI-5), определенный по методу БЭТ, составляет 0 21 мк, что соответствует наблюдаемому диаметру частиц. [40]
При получении красной окиси железа прокаливанием кристаллического железного купороса FeSO4 7Н2О обычно получается пигмент, содержащий большое количество крупных спекшихся частиц. Последняя и служит причиной появления в пигменте спекшихся частиц. Предупредить их образование можно предварительным обезвоживанием железного купороса, которое может происходить даже при комнатной температуре, хотя и очень медленно. Повышение температуры сильно ускоряет процесс: при 60 скорость обезвоживания становится достаточно заметной, а при 100 шесть молекул воды удаляются очень быстро. [41]
Для получения красной окиси железа применяют преимущественно сернокислую соль закиси железа ( железный купорос), значительно реже - сернокислую соль окиси железа. Железный купорос иногда прокаливают в смеси с мелом. [42]
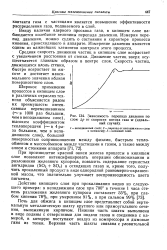 |
Зависимость перепада давления по слою Ар от скорости потока газа w ( идеальный случай. [43] |
При производстве красной окиси железа процессы в кипящем слое позволяют интенсифицировать операции обезвоживания и разложения железного купороса, повысить содержание сернистых ангидридов ( SO2 SO3) в отходящих газах и, кроме того, получить прокаленный продукте виде однородной равномерно-окрашенной массы, что значительно улучшает воспроизводимость цвета пигмента. [44]
Размер частиц красной окиси железа возрастает с переходом от светлых оттенков к темным и колеблется в пределах 0 1 - 0 8 и. Размер частиц и агрегатов под микроскопом составляет: 0 35 - 0 45 ц для светлых оттенков, 0 50 - 0 70 ц для средних, 1 0 - 1 5 ц для темных и 2 5 ц для пурпурных. Форма частиц светлых оттенков пластинчатая, темных - зернистая. [45]
Страницы: 1 2 3 4