Гидратированная окись
Cтраница 3
Гексабромоиридаты ( ГУ) выделяют из растворов гидратированной окиси иридия ( 1У) в бромистоводородной кислоте. Эти соли представляют собой кристаллы с глубокой синевато-черной окраской или темно-синие порошкообразные вещества, а растворы имеют ярко-синий цвет. Растворимость таких солей, как и в случае гек-сахлоридов, зависит от размера катиона. Ион [ 1гВгв ] 2 - также кинетически инертен, но отличается от фторидного и хлоридного аналогов тем, что в растворе не только медленно гидролизуется, но и разлагается с образованием свободного галогена. По-видимому, совершенно устойчивыми являются его растворы в разбавленной бромистоводородной кислоте, к которым добавлено небольшое количество брома. [31]
Из вышеизложенного следует, что мышьяковистая кислота [ гидратированная окись мышьяка As ( OH) 3 ] может вести себя в водном растворе и как кислота и как основание. [32]
Каталитической стадией реакции является окисление выпадающей в осадок гидратированной окиси Mri ( IV) до перманганата. [33]
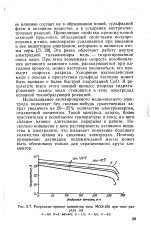 |
Разрядные кривые элементов типа МОЭ-250 при токе раз. [34] |
Это резко облегчает работу внутри электродной гальванопары медь - гидратированная окись меди. При этом возможная скорость возобновления активного закисного слоя, расходующегося при катодном процессе, может настолько увеличиться, что превысит скорость разряда. В результате всего этого ионный процесс разряда гидрати-рованной закиси меди становится в этих электродах основной токообразующей реакцией. [35]
Фосфорная кислота используется на таких носителях, как кизельгур или гидратированная окись алюминия. Смесь катализатора ( 70 - 85 %) и носителя нагревается до 200 - 350 С. Катализатор с фосфорной кислотой может постепенно терять свою активность вследствие дегидратации фосфорной кислоты в неактивную метафосфорную кислоту. [36]
В случае нейтральной окиси алюминия протоны возникают благодаря слабокислотной природе гидратированной окиси алюминия, которая в какой-то мере сохраняется даже после прокаливания при 500 С. Возможно, что все количество влаги в окиси алюминия после активирования находится на поверхности. Таким образом, поверхность окиси алюминия оказывается сильно гидратированной. Ионы фтора могут быть заменены отрицательными ионами соляной, серной, фосфорной и других кислот. Кислоты сильно адсорбируются окисью алюминия, и необходимы продолжительное нагревание и высокая температура, чтобы удалить эти вещества из окиси алюминия. [37]
Реакция с холодной водой приводит к выделению кислорода и образованию гидратированной окиси палладия PdO, тогда как при реакции с холодной концентрированной соляной кислотой происходит выделение хлора. Эти реакции подобны реакциям фторида кобальта CoF3, с которым PdF3 изоморфен, и характеризуют неустойчивость, присущую элементу в трехвалентном состоянии. Химия палладия подтверждает точку зрения, что нормальным является двухвалентное состояние. Это видно также из того, что для данного элемента неизвестен трихлорид. Так же как и трифторид кобальта, он может быть использован для фторирования органических соединений. [38]
В работе [ 573, № 520 ] показано, что гидратированная окись титана и основной карбонат цинка извлекают следы Pu ( IV) и ( VI) из карбонатных сред. [39]
Коллоидный плутоний ( IV) существует в виде катионных агрегатов гидроокиси или гидратированной окиси, состоящих из частиц большого молекулярного веса с небольшим положительным зарядом. Для осаждения плутония из таких полимеров осадителем типа оксалата, иодата, фосфата достаточно лишь 0 15 эквивалента осадителя. Это свидетельствует о небольшом числе остаточных зарядов в коллоидных агрегатах. Полимер, осажденный из солянокислого раствора, может быть легче отмыт от хлорид-ионов, которые, следовательно, не входят в решетку полимера. Связи в полимере осуществляются главным образом кислородными и гидроксильными мостиками. Определение молекулярного веса полимеров методом скоростного центрифугирования дает значение порядка сотен тысяч и даже миллионов. Коллоидная природа полимеров проявляется в сильной адсорбции их на стекле, бумаге, вате, поверхность которых в воде обладает отрицательным зарядом. [40]
Обычно приходится использовать, по существу, эмпирические методики получения разных типов гидратированной окиси алюминия - веществ, которые сами являются исходными для последующей дегидратации. Контролировать эти процессы нелегко, и имеющиеся в литературе указания иногда противоречивы. Если требуется определенная гидратированная форма, после получения желательно ее точно охарактеризовать. Де Бур и др. [41] приводят некоторые методики получения активной окиси алюминия, в частности образцов гиббсита и байерита ( имеющих состав А1 ( ОН) 3) с меняющейся реакционной способностью в отношении дегидратации. [41]
Растворы трибромида хрома окрашены в зеленый цвет; их можно получить растворением гидратированной окиси хрома ( Ш) в НВг при кипячении. [42]
Для реа кции дегидратации здесь имеют решающее значение относительно слабые бренстедовские кислотные центры гидратированной окиси алюминия, тогда как более сильные лью-исовские кислотные центры ответственны за перегруппировки углеродного скелета. [43]
К важнейшим соединениям марганца ( Ш) следует отнести безводную окись Мп203 или гидратированную окись МпООН, манга-ниты Меп [ Мп204 ], галогениды MnF3, МпС13, сульфат, квасцы, дифосфатоманганит, ацетат, гексациано -, оксалато -, малонатоман-ганиты, ацетилацетонат. Соединения марганца ( Ш) похожи на соединения железа ( Ш) склонностью к гидролизу, окислительными свойствами и тенденцией к образованию координационных соединений. [44]
Кислые золи цирконата можно также приготовить действием кислот, анионы которых способны к координации гидратированной окисью циркония. [45]
Страницы: 1 2 3 4