Непрореагировавшая окись - углерод
Cтраница 1
 |
Схема процесса получения янтарной кислоты из ацетилена и окиси углерода. [1] |
Непрореагировавшая окись углерода удаляется из верхней части реактора, проходит через холодильник 4, где конденсируются уносимые с газом пары растворителя, и возвращается в процесс. Сконденсировавшийся растворитель из сборника 3 также возвращается в реактор. Для предотвращения накопления побочных продуктов реакции ( пропионовой и акриловой кислот, циклопентанона) часть растворителя выводят из цикла и заменяют свежим. [2]
 |
Принципиальная схема синтеза пентакарбонила железа. [3] |
Образующиеся пары пентакарбонила железа вместе с непрореагировавшей окисью углерода очищаются от пыли в фильтре 6 и поступают в холодильник-конденсатор 7, где охлаждается реакционный газ и конденсируется карбонил. [4]
Как уже было отмечено, газообразные продукты реакции, помимо непрореагировавшей окиси углерода, содержат углекислоту. С целью предложить вероятный механизм реакции были отдельно изучены реакции разложения окиси углерода, формальдегида и гликолевой кислоты в присутствии 88 9 % - ного йодида никеля на силикагеле ( отношение никеля ксиликагелю 6: 4) при различных температурах и давлениях. Из полученных результатов, которые представлены в табл. 3 - 5, могут быть сделаны следующие выводы. [5]
Найдено, что газообразный продукт реакции представляет собой смесь углекислоты с непрореагировавшей окисью углерода. Другие газообразные продукты не были обнаружены с помощью стандартных методов газового анализа. [6]
При этих условиях в газе после реакции остается практически от 2 до 3 % непрореагировавшей окиси углерода. Схема процесса конверсии полуводяного газа представлена на фиг. Полуводяной газ из газгольдера 1 поступает в сатурационную башню 2, где происходит насыщение его водяным паром. Сатурационная башня представляет собой железный скруббер, заполненный насадкой. Газ проходит башню снизу вверх навстречу потоку горячей воды, нагревается за счет ее тепла и насыщается водяным паром. После сатурации на 1 объем полуводяного газа приходится ок. [7]
Не менее важно пропускание через катализатор равных объемов исходных газов и соблюдение такой скорости их пропускания, которая гарантирует наименьший проскок непрореагировавших окиси углерода и хлора. Несоблюдение этих условий при синтезе фосгена приводит к большим потерям продукта, который уносится вместе с иепрореаги-ровавшими газами. [8]
Реакция конверсии окиси углерода сопровождается тепловым эффектом 10 260 cal ( при 25) и является обратимой, при этом равновесие с повышением температуры сдвигается в сторону непрореагировавшей окиси углерода. [9]
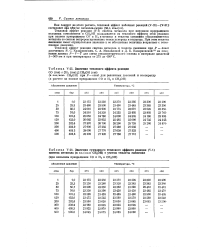 |
Значения теплового эффекта реакции.| Значения суммарного теплового эффекта реакции ( V-1 синтеза метанола ( в кал / моль СНаОН с учетом теплоты смешения. [10] |
Тепловой эффект реакции ( V-1) синтеза метанола при неполном превращении исходных компонентов в СН3ОН складывается из теплового эффекта этой реакции при полном превращении СО и Н, в метанол и теплоты смешения образовавшегося метанола со смесью непрореагировавших окиси углерода и водорода. При этом теплота вмешения имеет отрицательное значение и ее абсолютная величина возрастает с повышением давления. [11]
Технологическая схема процесса получения диметилформамида представлена на рис. 9.10. Осушенная смесь окиси углерода, диметиламина и метанола, содержащего катализатор - метилат натрия, пропускается через реактор карбонилирования 1, в котором происходит образование диметилформамида. Непрореагировавшая окись углерода выходит из верхней части реактора, охлаждается в холодильнике и компрессором 2 направляется на рециркуляцию. Жидкие продукты реакции после прохождения реактора дросселируются и поступают в колонну 3, где отгоняется избыток диметиламина, и направляется в рецикл. В колонне 4 происходит отгонка метанола от катализата диметилформамида, а в колонне 5 производится выделение товарного продукта. [12]
Затем из нее удаляют каталитические яды - двуокись углерода и сероводород - промывкой смеси моноэтаноламином или водой, хорошо растворяющей эти примеси под повышенным давлением. Выделившуюся из промывного раствора двуокись углерода используют в производстве мочевины, для конверсии метана [ см. уравнение реакции ( 2) ] или для получения сухого льда. От небольшого количества непрореагировавшей окиси углерода ( 0 3 - 0 5 % от объема газа) смесь освобождается в процессе предкатализа. Если в конвертор метана подается чистый кислород, то после конверсии окиси углерода и удаления двуокиси углерода газ промывают жидким азотом в колонне. [13]
Окись углерода представляет собой сильный яд. Опыты с ней нужно проводить под тягой. Только при получении небольших количеств окиси углерода в приборах, хорошо проверенных на герметичность, опыты можно проделывать без тяги. Но в этих случаях остатки непрореагировавшей окиси углерода сжигают или собирают над водой. [14]
Опыт проделывают так же, как и опыт восстановления окиси меди водородом - в пробирке, если его проводят под тягой. Без вытяжного шкафа окись меди насыпают в широкую стеклянную трубку, закрывают ее пробками с газоотводными трубками. Нагревают окись меди и с одного конца трубки пропускают окись углерода, с другого конца поджигают непрореагировавшую окись углерода. После охлаждения меди в слабом токе окиси углерода прекращают ее доступ, и учащимся показывают восстановленный металл. [15]
Страницы: 1 2