Характерное окрашивание
Cтраница 3
В других случаях применяют такие реактивы, которые вызывают характерное окрашивание исследуемого раствора. [31]
В других случаях применяют такие реактивы, которые вызывают характерное окрашивание исследуемого раствора. Например, при приливании раствора роданида калия к кислотному раствору какой-либо соли кобальта появляется интенсивное синее окрашивание, вызываемое образованием комплексного иона [ Co ( SCN) J - - ( см. гл. [32]
В других случаях применяют такие реактивы, которые вызывают характерное окрашивание исследуемого раствора. [33]
Типичной реакцией, позволяющей открыть небольшие количества фенолов, является характерное окрашивание, возникающее при действии хлорного железа. Фенол С6Н6ОН дает с хлорным железом фиолетовое окрашивание, с другими фенолами могут получаться другие оттенки. [34]
Более 100 лет известно, что лигнифицированные стенки клеток растений дают характерное окрашивание с определенными органическими и неорганическими реагентами. В 1834 г. Рунге [48] нашел, что при обработке еловой древесины фенолом и соляной кислотой на солнечном свету появляется зеленовато-синяя окраска, а при обработке сернокислым анилином - желтая окраска. Позднее было найдено большое количество реагентов, которые давали характерные цвета с лигнифицированными материалами. Эти реагенты могут быть классифицированы следующим образом: а) алифатические соединения, б) фенольные соединения, в) ароматические амины, г) гетероциклические соединения и е) неорганические реагенты. [35]
Фенолы, как одноатомные, так и многоатомные, дают - характерное окрашивание при добавлении раствора хлорного железа. Эта реакция является качественной пробой на фенол. [36]
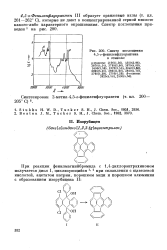 |
Спектр поглощения. [37] |
С), которые не дают в концентрированной серной кислоте какого-либо характерного окрашивания. [38]
Пары щелочных металлов ( простые вещества) и сложных соединений ЩЭ имеют характерное окрашивание: Li - карминово-красное, Na - желтое, К - фиолетово-розовое, Rb - беловато-розовое, Cs - фиолетово-розовое. Как известно, окраска пламени возникает в результате температурного возбуждения атома или иона, сопровождающегося перескоком электронов на более высоко лежащие энергетические уровни. [39]
Дальнейшее развитие этого раздела аналитической химии поз водило прийти к заключению, что характерные окрашивания осадков получаются у ряда ионов только с теми органическими реактивами, в молекулах которых имеются определенные атомные группировки. [40]
В качестве детектирующих реактивов общего назначения пригодны также трихлорид и пентахлорид сурьмы, дающие характерное окрашивание со многими соединениями. Пентахлорид сурьмы используется в виде 10 - 20 % - ного раствора в че-тыреххлористом углероде [33], а трихлорид - в виде насыщенного раствора в хлороформе, не содержащем спирта. После опрыскивания одним из этих растворов пластинки нагревают 5 - 10 мин при 100 - 120 С. Рейхельт и Питра [34] применили для той же цели насыщенный раствор трихлорида сурьмы в не содержащем спирта хлороформе с добавкой 20 % уксусного ангидрида. [41]
Интересен метод титрования Се4 ферроцианидом калия [731] в присутствии метиленовой сини, которая дает характерное окрашивание с ионами Се4, в то время как с Се3 такого окрашивания не образуется. Метод позволяет определять Се в присутствии других элементов третьей группы. [42]
Реакция основана на способности стрептомицина гидролизо-ваться щелочью с образованием мальтола ( а-метил-р-оксипирона), дающего характерное окрашивание с ионами трехвалентного железа. [43]
Папаверин, являясь производным замещенного фенола, вступает в окислительно-восстановительные реакции, а также дает характерное окрашивание с некоторыми реактивами, так, например, смесь формальдегидсерной кислоты с папаверином дает характерное красное окрашивание ( обычно его называют виннокрас-ным), которое переходит в желтое, грязно-коричневое и, наконец, в ярко-оранжевое. В присутствии раствора гексациано - ( П) - фер-риата, перманганата калия или фосфорномолибденовой кислоты появляется синяя окраска, переходящая последовательно в фиолетовую, зеленую, грязно-коричнево-желтую. [44]
Щелочные дитиокамфокарбонаты очень легко растворимы в воде и дают с большинством солей тяжелых металлов осадки или характерное окрашивание. Соль меди имеет темнокоричневый цвет, совершенно отличный от ксантогенатов меди, которые, как известно, очень характерны. [45]
Страницы: 1 2 3 4