Оксалат - кадмий
Cтраница 1
Оксалат кадмия CdC204 ЗН20 осаждается при действии оксалатов или щавелевой кислоты. [1]
Процесс получения красного кадмия прокаливанием смеси карбоната или оксалата кадмия с серой и селеном состоит из следующих операций: изготовление и прокаливание шихты; промывка, фильтрование и сушка прокаленной массы. [2]
Реакции на кадмий и марганец со щавелевой кислотой ведут к образованию оксалатов кадмия СдС2О4 ЗН2О и марганца МпС2О4 - ЗН2О в виде бесцветных призм и параллелограммов, сходных по внешнему виду. Для их различия можно использовать очень сильное двупреломление и прямое погасание кристаллов оксалата марганца в отличие от косого погасания и значительно более слабого двупреломления кристаллов оксалата кадмия ( гл. [3]
Предлагают также [503] определять кальций полярографи-рованием ионов кадмия, вытесненных кальцием из оксалата кадмия. Полярографируют в 0 1 N растворе К. [4]
Предлагают также [503] определять кальций полярографи-рованием ионов кадмия, вытесненных кальцием из оксалата кадмия. [5]
Для получения кадмиевых пигментов применяют твердофазный прокалбчный способ - шихту из карбоната или оксалата кадмия и серы прокаливают без доступа воздуха при 600 С. [6]
Для получения кадмиевых пигментов применяют твердофазный прокалочный способ - шихту из карбоната или оксалата кадмия и серы прокаливают без доступа воздуха при 600 С. [7]
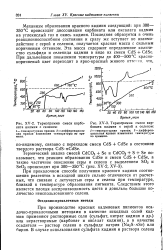 |
Термограмма смеси карбоната кадмия с селеном.| Термограмма смеси карбоната кадмия с серой и селеном. [8] |
Механизм образования красного кадмия следующий: при 300 - 350 С происходит диссоциация карбоната или оксалата кадмия на углекислый газ и окись кадмия. Последняя образуется в очень реакционноспособном состоянии и сразу же вступает во взаимодействие с серой и селеном, получается красная масса с сильным коричневым оттенком. [9]
Разработано 5 амперометрическое определение кальция при помощи оксалата с использованием твердофазной реакции: к соли кальция в 0 1 М растворе хлорида калия добавляют твердый оксалат кадмия; так как оксалат кальция значительно менее растворим, чем оксалат кадмия, то из твердой фазы выделяется кадмий, количество которого строго эквивалентно количеству кальция в растворе. Освободившиеся ионы кадмия титруют раствором ферроцианида калия ( см. раздел Кадмий) по току восстановления кадмия на ртутном капельном электроде; в качестве анода был применен ртутный донный электрод. [10]
При прокалочном способе синтеза реакция между окисью кадмия или диссоциирующими при невысокой температуре ( до 400 С) солями кадмия ( например, карбонатом и оксалатом кадмия) и серой протекает в твердой фазе. [11]
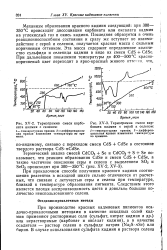 |
Термограмма смеси карбоната кадмия с селеном.| Термограмма смеси карбоната кадмия с серой и селеном. [12] |
При производстве красных кадмиевых пигментов оса-дочно-прокалочными методами в качестве исходных солей кадмия применяют растворимые соли ( сульфат, нитрат кадмия и др.) или нерастворимые ( карбонат и оксалат кадмия), а в качестве осадителя - раствор селена в сульфиде натрия ( Na2S - nSe) или бария. [13]
Разработано 5 амперометрическое определение кальция при помощи оксалата с использованием твердофазной реакции: к соли кальция в 0 1 М растворе хлорида калия добавляют твердый оксалат кадмия; так как оксалат кальция значительно менее растворим, чем оксалат кадмия, то из твердой фазы выделяется кадмий, количество которого строго эквивалентно количеству кальция в растворе. Освободившиеся ионы кадмия титруют раствором ферроцианида калия ( см. раздел Кадмий) по току восстановления кадмия на ртутном капельном электроде; в качестве анода был применен ртутный донный электрод. [14]
Менее возможно, но не исключено также получение фигуры любого другого разреза. Так, например, триклинный оксалат кадмия образует кристаллы, многие из которых в сходящемся свете дают фигуру разреза, почти перпендикулярного к оптической оси, притом в поле зрения виден также выход ОБ. Фигура разреза, перпендикулярного к оптической оси, наблюдается почти у всех кристаллов бихромата серебра. [15]
Страницы: 1 2