Комплексный оксалат
Cтраница 3
Для Zn и Cd характерны кристаллогидраты ZnCaO4 2H2O и CdCaO4 ЗН О. Производящиеся от них комплексные оксалаты принадлежат главным образом к тину AVzlSfQiOibL где М - одновалентный металл. [31]
Так, при образовании комплексного оксалата к положительно заряженному центральному иону металла присоединяются ионы С2О42 -, а в этилендиами-новом комплексе связь образуется по донорно-акцепторному механизму - за счет донорных свойств атомов азота. [32]
Так, при образовании комплексного оксалата к положительно заряженному центральному иону металла присоединяются ионы С2О -, а в этилен-диаминовом комплексе связь образуется по донорно-акцепторному механизму - за счет донорных свойств атомов азота. [33]
Растворы нагревают до 60 С и добавляют избыток насыщенного раствора щавелевой кислоты. Образовавшийся осадок оксалатов отфильтровывают; в растворе содержатся хорошо растворимые комплексные оксалаты железа, алюминия и урана. Осадки на фильтре воронки Бюхнера сначала промывают разбавленными растворами щавелевой и минеральной ( H2SO4, HNO3, HC1) кислот для удаления соосажденных фосфатов и адсорбированной НзРО4, а затем водой. Оксалаты редкоземельных элементов превращаются в нерастворимые двойные карбонаты и остаются в осадке. [34]
Некоторые из этих соединений образуются при действии избытка осадителя на соответствующий осадок - например комплексные оксалаты, тартраты, цитраты. [35]
Метод дробной кристаллизации основан на использовании различия в растворимости устойчивых соединений циркония и гафния - оксихлоридов, сульфатов, комплексных оксалатов и фторидов, не разрушающихся при многочисленных перекристаллизациях. Наиболее подходящи для разделения фтороцирконаты и фторогафнаты калия. Соотношение между раствор имостями других комплексных фторидов значительно меньше. [36]
Можно было бы думать, что скорость окисления щавелевой кислоты сильно возрастает, если к раствору прибавить большой избыток индуктора - соли двухвалентного марганца. Однако это не так; хотя реакция между перманганатом и ионами Мп44 проходит при этом быстро, продуктом реакции является главным образом комплексный оксалат трехвалентного марганца, который разлагается с измеримой скоростью. [37]
Кроме того, для висмута известны комплексы с серусодержащими лигандами, например с тиомочевиной. Комплексы типа двойных солей с анионами кислородных кислот, практически неизвестные для мышьяка, уже известны для сурьмы, например Me [ Sb ( S04) 2 ] и более устойчивы в случае висмута: Me [ Bi ( S04) 2 ], Me3 [ Bi ( S04) 3 ] и др. Для Bi ( III) известны также комплексные оксалаты, пирофос-фаты и роданиды. [38]
Для количественного разделения циркония и гафния достаточно удовлетворительных методов неизвестно, Для этой цели предложен метод ионного обмена. Комплексные оксалаты, а также фториды циркония и гафния были хроматографически разделены на анионите. Для очистки циркония и разделения циркония и гафния предложены 34 также и некоторые другие способы, основанные на ионном обмене. [39]
Оксалат бериллия - BeCjO4 ЗН2О - является единственным оксалатом двухвалентного металла, хорошо растворимым в воде. Электропроводность его разбавленного раствора примерно в 5 раз меньше, чем у BeSO4, и почти не изменяется при повышении концентрации. Известны и комплексные оксалаты, например Ка. [40]
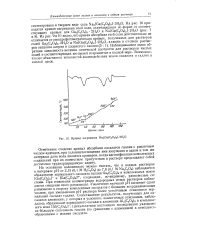 |
Кривая нагревания Ыа3 [ Оа ( С2О4 з ]. ЗН2О. [41] |
На основании изложенного можно считать, что в водных растворах в интервале рН от 2 15 ( 0 1 М Н2С2О4) до 7 8 ( 0 1 М Na2C2O4) наблюдается образование нормального оксалата галлия Ga2 ( C2O4) 3 и комплексных ионов [ Ga ( C2O4) 2 ] - и [ Ga ( C2O4) 3 ] 3 -, создающих, по-видимому, равновесные системы. При изменении концентрации водородных ионов растворов наблюдается смещение этого равновесия. Увеличение значений рН вызывает сдвиг равновесия в сторону комплексных оксалатов с большим координационным числом; при уменьшении рН раствора более устойчивым становится нормальный оксалат галлия. Сопоставление результатов, полученных для оксалатов алюминия, у которых в условиях, аналогичных описанным, наблюдалось образование нормального оксалата алюминия А12 ( С2О4) 3 и комплексного иона [ А1 ( С2О4) 2Г, с результатами настоящего исследования указывает на большую склонность галлия ( по сравнению с алюминием) к комплексо-образованию с ионами оксалата. [42]
Интересно, что хромовые соли разлагаются уже под действием рассеянного света или при слабом нагревании. Кобальтовые соли термически сравнительно устойчивы и не распадаются до 160 - 200 С. По данным ИК-спектроскопии в присоединенных группах С2О4 - в оксалатах германия, как и в других комплексных оксалатах, понижается симметрия. [43]
В этом случае алюминий, хром, марганец, железо и другие катионы маскируются в виде комплексных оксалатов, легко растворимых в воде. Некоторые катионы тяжелых металлов - серебро, сурьма, ртуть, свинец, висмут не дают растворимых оксалатных комплексов, но осаждаются металлическим цинком. В раствор переходит ион цинка, не мешающий реакции на кальций и образующий комплексный оксалат. Стронций и барий не мешают реакции, так как осаждаются в виде сульфатов; растворимость сульфата кальция 2 5 г. л, что позволяет уверенно обнаружить кальций в фильтрате в виде оксалата кальция после осаждения мешающих катионов. [44]
Методика состоит в следующем: смесь окислов редкоземельных элементов, содержащую церий, растворяют в концентрированной H2S04, раствор разбавляют водой и пересыщают аммиаком в присутствии уксусной кислоты. Полученную желтую жидкость вливают при взбалтывании в избыток раствора щавелевокислого аммония, при этом цвет жидкости темнеет. Получается осадок оксалатов закиси церия, окиси лантана и др., а отфильтрованный раствор представляет собой темнооранже-вую или красную жидкость и заключает в себе комплексный оксалат окиси церия. [45]
Страницы: 1 2 3 4