Оксид - щелочной металл
Cтраница 1
Оксиды щелочных металлов - очень реакционноспособные вещества, энергично взаимодействуют с водой, образуя гидроксиды. [1]
Оксиды щелочных металлов - твердые, - сильно гигроскопичные вещества. Они легко соединяются с водой, образуя гидроксиды - твердые вещества, хорошо растворимые в воде. Соли щелочных металлов, как правило, тоже хорошо растворяются в воде. [2]
Оксиды щелочных металлов М2О являются типичными основными оксидами, а гидроксиды МОН - щелочами, которые хорошо растворимы в воде и создают сильнощелочную среду. [3]
Оксиды щелочных металлов должны быть гетерополярными, так как температуры плавления их очень высоки. [4]
 |
Схема молекул оксида и пероксида натрия. [5] |
Оксиды щелочных металлов энергично образуются при непосредственном контакте металлов с кислородом воздуха, поэтому щелочные металлы хранят в вакууме или под слоем углеводородов ( керосин), но и при этом со временем они покрываются оксидным слоем за счет диффузии кислорода. [6]
Оксиды щелочных металлов МзО являются типичными основными оксидами, а гидроксиды - щелочами, которые хорошо растворимы в воде и создают сильнощелочную среду. Оксиды и гидроксиды элементов ПА-группы ( кроме бериллия) проявляют основные свойства; гидроксиды стронция и бария из-за хорошей растворимости в воде можно называть щелочами аналогично гид-роксидам щелочных металлов. [7]
Оксиды щелочных металлов ( Na2O, K2O, П2О) играют роль плавней, снижая температуру плавления стекольной шихты и вязкость расплава. Они повышают плотность, ТКЛР, диэлектрическую проницаемость и снижают химическую стойкость, электросопротивление стекла. [8]
Оксиды щелочных металлов исследованы для восстановления оксидов азота в сочетании с соединениями элементов других групп без носителя или на носителе. [9]
Оксиды щелочных металлов снижают вязкость, температуру размягчения, механическую прочность и твердость стекол. Оксиды щелочно-земельных металлов позволяют регулировать вязкость стеклянных расплавов в заданных пределах. Кислотные оксиды повышают механическую прочность, термическую и химическую стойкость стекол. [10]
Оксиды щелочных металлов Э2О - это кристаллические термически устойчивые вещества, при взаимодействии с водой образуют щелочи. [11]
Оксиды щелочных металлов энергично образуются при непосредственном контакте металлов с кислородом воздуха, поэтому щелочные металлы хранят или в вакууме, или под слоем углеводородов ( керосин) и то со временем за счет диффузии кислорода они покрываются оксидным слоем. [12]
Оксидами щелочных металлов промотируют также У2О5 - пром. [13]
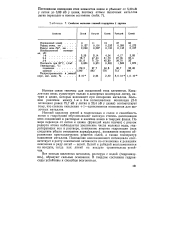 |
Свойства металлов главной подгруппы I группы. [14] |
Все оксиды щелочных металлов, реагируя с водой ( гидролизу-ясь), образуют сильные основания. В твердом состоянии гидрок-сиды устойчивы и способны возгоняться. [15]
Страницы: 1 2 3 4