Оксид - серебро
Cтраница 1
Оксид серебра содержит 93 05 вес. Чему равна атомная масса серебра. [1]
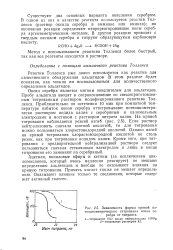 |
Зависимость формы кривой по-тенциометрического титрования ионов серебра от титранта. [2] |
Оксид серебра является мягким окислителем для альдегидов. Пробу альдегида вводят в соприкосновение со свежеприготовленным титрованным раствором модифицированного реактива Толленса. Приблизительно по истечении 10 мин при комнатной температуре избыток ионов серебра оттитровывают потенциометри-чески раствором иодида калия с серебряным и каломельным электродами и мостиком с раствором нитрата калия. [3]
Оксид серебра ( AgiO) применяется для очистки питьевой воды, для полирования и тонирования желтого стекла в стекольной промышленности и как катализатор. В ветеринарной медицине он используется в виде мази или раствора в качестве бактерицидного средства и для борьбы с паразитами. Оксид серебра - сильный окислитель и огнеопасен. [4]
Оксид серебра всегда готовят непосредственно перед опытом, добавляя к раствору нитрата серебра раствор гидроксида щелочного металла. [5]
Оксид серебра ( 1) Ag2O выпадает из растворов солей серебра при действии щелочен в виде коричневого осадка. [6]
Оксид серебра разлагается на воздухе при температурах выше комнатной. [7]
Оксид серебра ( П) рекомендован [46] для окисления Мп11 до перманганата, хрома ( III) до бихромата и Се111 до CeIV в кислом растворе. [8]
Оксид серебра () Ag2O почти нерастворим в воде и соединяется с ней в ничтожной степени с образованием гидроксида AgOH, который представляет собой более сильное основание, чем гидроксиды меди. [9]
Оксид серебра разлагается на воздухе при температурах выше комнатной. [10]
Оксид серебра ( II) образуется при окислении серебра озоном. [11]
Оксиды серебра имеют электрическую проводимость, близкую к проводимости чистого серебра. При повышенных температурах они разрушаются. Поэтому переходное сопротивление контактов из серебра, а также из серебросодержащих мегаллокерамик практически не изменяется с течением времени. Оно даже может понизиться вследствие медленной пластической деформации материала в площадках контактирования. Для медных контактов необходимо применять меры борьбы с окислением их рабочих поверхностей. [12]
Оксид серебра Ag2O и оксид ртути ( I) HgjO нерастворимы в избытке щелочи, но растворимы в азотной кислоте. [13]
Оксиды серебра используются, inter alia, в производстве электрических источников питания. [14]
Оксид серебра ( 1) в малой степени реагирует с водой с получением катиона ( КЧ Ag1 в аквакомплексе не установлено) и гидроксид-иона. [15]
Страницы: 1 2 3 4