Оксид - углерод
Cтраница 1
Оксид углерода ( IV), сероводород, оксид серы ( IV) и кислород - наиболее часто присутствующие в воде, вредные коррози-онноспособные газы. Поэтому воду анализируют на их содержание. Оксид углерода ( IV) всегда присутствует в воде. [1]
Оксид углерода ( II) может выступать в роли лиганда в комплексных соединениях. Присоединяясь к гемоглобину крови, моноксид углерода тем самым лишает его способности переносить кислород - с этим связано токсическое действие СО на человека и тех животных, в крови которых содержится гемоглобин. [2]
Оксид углерода ( IV) в сочетании с гидрокарбонатами обусловливает буферные свойства воды. Угольная кислота встречается в природных водах в форме недиссоциированных молекул Р СОз, гидрокарбонатных НСОз и карбонатных СОз2 - ионов. Форму содержащейся в воде угольной кислоты, диссоциирующей ступенчато, можно определить по константам диссоциации. [3]
Оксид углерода, цианистый водород и нитрилы также реагируют с ароматическими соединениями в присутствии сильных кислот или других катализаторов Фриделя-Крафтса. Эти реакции широко используются в синтезах, поскольку в результате образуются формил - и ацил-замещенные ароматические соединения. Эти электроноакцепторные группы препятствуют дальнейшему электрофильному замещению. [4]
Оксиды углерода и азота, сероводород являются сильными ядами. Диоксид серы, находясь в воздухе, окисляется до триоксида серы, который при взаимодействии с атмосферной водой образует серную кислоту. Последняя наносит вред растениям, подкисляет почву, ускоряет процесс коррозии металлов, разрушает каменную облицовку зданий. [5]
Оксид углерода ( IV), образующийся при полном сгорании 0 1 моль предельного углеводорода, дает 60 г осадка при пропускании его в избыток известковой воды. Определите молекулярную формулу и строение предельного углеводорода, если известно, что он содержит одни четвертичный атом углерода. [6]
Оксид углерода вызывает пористость при недостаточной рас-кисленности металла сварочной ванны. [7]
Оксид углерода используется вместо водорода в случае с медью [5, 8], на которой водород адсорбируется медленно. К тому же, существенная адсорбция оксида углерода происходит и на носителе, что требует корректировок, часто таких же значительных, как при хемосорбции на металлах в разбавленных системах. [8]
Оксид углерода при контакте с оксидами железа огеупорного материала, являющегося в данном случае катализатором, разлагается по реакции 2СО СО2 С. В результате этой реакции выделяется сажистый углерод. [9]
Оксид углерода также может выходить из печных бункеров при их недостаточном заполнении. [10]
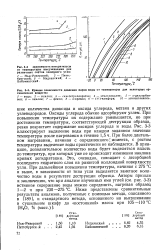 |
Кривые зависимости давления паров воды от температуры для некоторых органических веществ. [11] |
Оксиды углерода обычно адсорбируют углем. При повышении температуры их содержание уменьшается, но при достижении температуры, соответствующей деструкции образца, резко возрастает содержание оксидов углерода и воды. При более длительном нагревании, начиная с определенного J момента, с ростом температуры выделение воды практически не наблюдается. В принципе, дополнительное количество воды будет выделяться вплоть до температур, при которых уже не происходит изменения наклона кривых дегидратации. Это, очевидно, совпадает с десорбцией последнего гидратного слоя на развитой коллоидной поверхности угля. При дальнейшем повышении температуры, начиная с 275 С и выше, в зависимости от типа угля выделяется заметное количество воды в результате деструкции образца. [12]
Оксид углерода ( СО) является бесцветным газом без запаха, который снижает способность гемоглобина переносить и поставлять кислород. [13]
Оксид углерода получается при сжигании органического материала типа угля, древесины, бумаги, масла, бензина, газа, взрывчатых веществ или карбонатных материалов любого другого типа в условиях недостатка воздуха или кислорода. Когда процесс горения происходит при избыточном питании воздухом и пламя не контактирует с какими-либо поверхностями, окись углерода не образуется. СО образуется в том случае, если пламя контактирует с поверхностью, температура которой ниже, чем температура воспламенения газообразной части пламени. На двигатели транспортных средств приходится от 55 до 60 % всего количества СО искусственного происхождения. Выхлопной газ бензинового двигателя ( электрическое зажигание) является обычным источником образования СО. Выхлопной газ дизельного двигателя ( компрессионное воспламенение) содержит приблизительно 0 1 % СО, если двигатель работает надлежащим образом, однако неправильно отрегулированный, перегруженный или технически плохо обслуживаемый дизельный двигатель может выбрасывать значительные количества СО. Тепловые или каталитические дожигатели в выхлопных трубах значительно снижают количество СО. Другими основными источниками СО являются литейные производства, установки каталитического крекинга на нефтеперерабатывающих предприятиях, процессы дистилляции угля и древесины, известеобжигательные печи и печи восстановления на заводах крафт-бумаги, производство синтетического метанола и других органических соединений из оксида углерода, спекание загрузочного сырья доменной печи, производство карбида, производство формальдегида, заводы технического углерода, коксовые батареи, газовые предприятия и заводы по переработке отходов. [14]
Оксид углерода производится в промышленных масштабах путем неполного окисления газообразных углеводородов из природного газа или газификацией угля или кокса. Он используется как восстановитель в металлургии, в органическом синтезе, производстве карбонилов металла. Некоторые газы промышленного использования, применяемые для подогрева котлов и печей, а также питания газовых двигателей, содержат оксид углерода. [15]
Страницы: 1 2 3 4