Оксид - церие
Cтраница 2
Другим ярким примером пестехиометрни служат оксиды лантаноида, имеющие вакансии по кислороду. Например, для оксидов церия, празеодима, тербия характерна структура флюорита, но цвет этих оксидов и другие свойства различны: СеО2 имеет бледно-желтую окраску, РгО2 - черную, ТЮ2 - коричневую. Окраска ТЬО2 и РгО2 объясняется нарушением стехиометрии из-за недостатка кислорода. Оксид церия СеО2устойчив во всей области температур при атмосферном давлении; давление, необходимое для получения РгО2, достигает 105 Па при температуре 310 С. Оксид тербия может быть получен только при действии атомного кислорода на оксиды с низшей степенью окисления. Изучение структуры этих оксидов показало, что в зависимости от содержания кислорода может быть много индивидуальных соединений. [16]
Токсические свойства лантаноидов проявляются в замедлении свертываемости крови, хронических фарингитах и ринитах - заболеваниях верхних дыхательных путей. У работающих с оксидом церия ( IV) на производстве полирующего состава - поляри-та наблюдаются при непосредственном контакте кожные дерматиты. [17]
Непрерывный процесс разложения воды описан в патенте США № 4053576, 19.05.75. Основой его является устройство для концентрирования солнечной энергии с целью обеспечения температуры до 3000 К в зоне реакции. Капсулу-мембрану, изготовленную из оксидов церия, гафния, стронция, циркония, селективно проницаемую для водорода и находящуюся в фокусе параболического зеркала, размещают в камере, изготовленной из газонепроницаемого прозрачного материала. В этой камере под действием света происходит частичная диссоциация водяного пара, и получаемый водород диффундирует через водородопроницаемую мембрану. Кислород вместе с частью непрореагировавшего пара удаляется из камеры диссоциации. Расчеты показали [494], что для получения приемлемых характеристик процесса необходимо несколько ступеней разделения водорода и кислорода. [18]
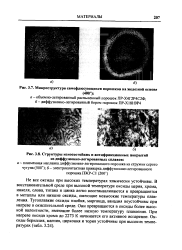 |
Структуры износостойких и антифрикционных покрытий из диффузионно-легированных сплавов. [19] |
Не все оксиды при высоких температурах химически устойчивы. В восстановительной среде при высокой температуре оксиды церия, хрома, никеля, олова, титана и цинка легко восстанавливаются и превращаются в металлы или низшие оксиды, имеющие невысокие температуры плавления. Тугоплавкие оксиды ниобия, марганца, ванадия неустойчивы при нагреве в окислительной среде. Они превращаются в оксиды более высокой валентности, имеющие более низкую температуру плавления. При нафеве оксида хрома до 2273 К начинается его активное испарение. [20]
Раствор формальдегида в серной кислоте в присутствии гексацианоферрата ( III) калия дает синюю окраску, переходящую последовательно в фиолетовую, зеленую, грязную коричнево-желтую. Папаверин дает подобные цветные реакции и при использовании вместо гексацианоферрата ( III) оксида церия ( IV), пер-манганата калия или фосфорномолибденовой кислоты. [21]
Приготовленные растворы должны содержать высокую концентрацию кислоты, обычно 1 М или больше, для предотвращения осаждения гидрата оксида церия. [22]
Оксиды РЗЭ обладают основными свойствами, мало-растворимы в воде. Оксид лантана, обладающий наиболее основными свойствами, показывает щелочную реакцию воды. Оксиды РЗЭ, за исключением оксида церия ( IV) СеО2, хорошо растворяются в кислотах, даже в слабой уксусной кислоте. Оксид церия ( IV) растворяется в горячей серной. [23]
Соединения РЗЭ подгруппы Y более токсичны, чем соединения подгруппы Се; оксиды менее токсичны, чем соли соответствующих металлов; видовые различия мышей и крыс к изученным соединениям отсутствуют. По результатам опытов с введением в желудок изученные соединения отнесены к уме-ренно - и малоопасным веществам; по результатам опытов с в / брюшинным введением - к малотоксичным и практически нетоксичным. В то же время при однократном 4-часовом вдыхании оксида церия ( IV) и оксида иттрия пороги острого ингаляционного действия для крыс составляют соответственно 95 и 92 мг / м3, что позволило по степени опасности однократного ингаляционного воздействия отнести эти соединения к высокоопасным веществам. При введении 50 мг Y2O3 интратрахеально крысам через 9 мес. Андреева и др. указывают, что при в / брюшинном введении РЗЭ мышам и морским свинкам наблюдалось развитие разлитого перитонита. [24]
Кремнистая лигатура РЗМ для модифицирования ковкого и серого чугунов имеет состав: 9 - 11 % Се, 36 - 40 % Si, остальное железо. Шихта включает кварцит, древесную щепу, окатыши гидрата оксида церия и низкозольный уголь. Количество восстановителя в шихте составляет 98 - 100 % от теоретически необходимого. [25]
Полирование пластин производят на мягких подложках из фетра, велюра или батиста, пропитанных абразивными пастами на жировой основе с крупностью зерен абразива от 3 до 0 25 мкм. Класс чистоты полученной поверхности соответствует V14 и выше. При полировании полупроводниковых пластин используют алмазные порошки и пасты, пасты на основе кубического нитрида бора ( эльбора), оксида алюминия, оксидов церия, циркония, хрома, кремния. [26]
Другим ярким примером пестехиометрни служат оксиды лантаноида, имеющие вакансии по кислороду. Например, для оксидов церия, празеодима, тербия характерна структура флюорита, но цвет этих оксидов и другие свойства различны: СеО2 имеет бледно-желтую окраску, РгО2 - черную, ТЮ2 - коричневую. Окраска ТЬО2 и РгО2 объясняется нарушением стехиометрии из-за недостатка кислорода. Оксид церия СеО2устойчив во всей области температур при атмосферном давлении; давление, необходимое для получения РгО2, достигает 105 Па при температуре 310 С. Оксид тербия может быть получен только при действии атомного кислорода на оксиды с низшей степенью окисления. Изучение структуры этих оксидов показало, что в зависимости от содержания кислорода может быть много индивидуальных соединений. [27]
Оксиды РЗЭ обладают основными свойствами, мало-растворимы в воде. Оксид лантана, обладающий наиболее основными свойствами, показывает щелочную реакцию воды. Оксиды РЗЭ, за исключением оксида церия ( IV) СеО2, хорошо растворяются в кислотах, даже в слабой уксусной кислоте. Оксид церия ( IV) растворяется в горячей серной. [28]
При замене в шихте, рассчитанной на получение коллоидно-окрашенных стекол, компонентов-восстановителей на оптические сенсибилизаторы создаются возможности для получения фоточувствительных стекол. После варки и охлаждения до комнатной температуры такие стекла бесцветны и прозрачны. После ультрафиолетового или другого облучения и последующей тепловой обработки в стекле образуется окрашенное изображение. Наиболее часто в качестве сенсибилизатора используют оксид церия. [29]
Оксиды РЗЭ получают прокаливанием кислородсодержащих соединений ( нитраты, оксалаты, сульфаты, гидроксиды); они также образуются при взаимодействии металлов с кислородом воздуха при 180 - 200 С. Хлорид скандия получают взаимодействием оксида скандия с хлором при температуре выше 800 С. Галогениды РЗЭ образуются также из металлов в результате реакции их с галогенами. Фторид церия ( III) получают взаимодействием оксида, гидроксида или карбоната церия ( III) с фтористоводородной кислотой либо оксида церия ( IV) с фтористоводородной кислотой при 400 С. Сульфиды РЗЭ получаются при нагревании металлов с парами серы. [30]
Страницы: 1 2 3