Кислотный оксид
Cтраница 3
Некоторые кислотные оксиды с водой не взаимодействуют. Однако сами они могут быть получены из соответствующей кислоты. [31]
Некоторые кислотные оксиды с водой не реагируют. [32]
Многие кислотные оксиды при нагревании реагируют с основными оксидами с образованием солей. [33]
Некоторые кислотные оксиды с водой не взаимодействуют. [34]
Как кислотный оксид SiO2 взаимодействует с основаниями. Наибольшей агрессивностью обладают едкие щелочи NaOH и КОН. [35]
Некоторые кислотные оксиды, взаимодействуя с водой, могут присоединять разное число молекул воды, образуя кислоты различного состава. [36]
Некоторые кислотные оксиды, например оксид кремния, с водой не взаимодействуют, однако им также соответствуют кислоты. [37]
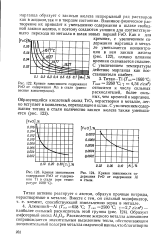
Образующийся кислотный оксид ТЮ2 нерастворим в металле, легко вступает в комплексы, переходящие в шлак. [39]
Все кислотные оксиды реагируют со щелочами ( см. ниже), образуя соль и воду, но иногда такая реакция при комн -: юй температуре идет очень медленно, например в случае оксида кремния. Очень медленно протекают реакции между кислотными оксидами и малорастворпмыми основаниями. [40]
Все кислотные оксиды, кроме SiO2, растворимы в воде. Амфотер-ные оксиды не растворяются в воде. [41]
Как кислотный оксид SiO2 при нагревании или сплавлении реагирует с основными оксидами, щелочами и некоторыми солями ( например, карбонатами) с образованием солей кремниевой кислоты - силикатов. [42]
Все кислотные оксиды, кроме SiO2, растворяются в воде. [43]
Некоторые кислотные оксиды, например оксид кремния, с водой не взаимодействуют, однако им также соответствуют кислоты. [44]
Все кислотные оксиды реагируют со щелочами ( см. ниже), образуя соль и воду, но иногда такая реакция при комн -: юй температуре идет очень медленно, например в случае оксида кремния. Очень медленно протекают реакции между кислотными оксидами и малорастворпмыми основаниями. [45]
Страницы: 1 2 3