Твердый оксид
Cтраница 4
Наряду с соединениями постоянного состава, для которых справедливы законы постоянства состава и кратных отношении, существуют соединения переменного состава. К последним относятся, например, многие твердые оксиды, сульфиды, нитриды, карбиды и пр. [46]
 |
Остов ионного соединения. [47] |
Обменное взаимодействие анионов играет структуроформирующую роль не только в строении гало-генидов, но и многих других неорганических веществ. Это относится, например, к таким важным классам вещества, как твердые оксиды, сульфиды, вообще халькогениды, а также силикаты, алюмосиликаты и др. Остов оксидов образуется благодаря обменному взаимодействию оксоионов. При этом он определяет тип их структуры, природу соединений. Это видно на примере довольно странных на первый взгляд соединений вроде СаТЮз - не то солей, не то оксидов. [48]
 |
Хлорирование борного ангидрида в присутствии твердого восстановителя. [49] |
Расплавленный В203 обладает значительной вязкостью, имеет неизмеримо меньшую удельную поверхность, чем высокодисперсный твердый оксид, вследствие чего ухудшаются условия контакта между газообразным оксидом углерода и борным ангидридом. Твердый восстановитель ( размер частиц 0 1 мм) способствует хорошему контактированию хлора и расплавленного оксида бора. Функцию центра встречи трех компонентов принимает на себя восстановитель с высокоразвитой поверхностью. [50]
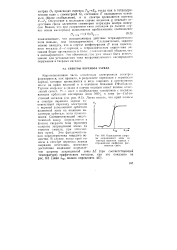 |
Определение шири-чы запрещенной зоны по спектру переноса заряда в отраженном диффузно рассеянном свете. [51] |
Это обстоятельство уже может быть использовано для установления типа координационного кислородного окружения в твердых оксидах. [52]
Так, например, теллурово-дород разлагается уже при комнатной температуре, подвергаясь реакции внутримолекулярного окисления-восстановления. Напротив, теплота образования кислородных соединений и их химическая стойкость возрастают, например АЯ0бр для твердых оксидов равна для SeO2 - 53 9 ккал / моль, а для ТеО2 - 76 2 ккал / моль. Известно, что чем сильнее выражены металлические свойства элемента, тем менее стойко его водородное соединение и более стойко кислородное. [53]
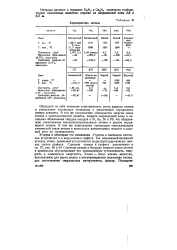 |
Характеристика оксидов. [54] |
Обращают на себя внимание сопряженность роста радиуса атомов и уменьшение потенциала ионизации с увеличением порядкового номера элемента. В том же направлении уменьшается энергия связи атомов в кристаллической решетке, ширина запрещенной зоны и энтальпия образования твердых оксидов у Si, Ge, Sn и Pb, что обусловлено уменьшением электроотрицательности атомов с ростом порядкового номера. В том же направлении происходит металлизация химической связи атомов в кристаллах элементарных веществ и сильный рост их проводимости. [55]
Страницы: 1 2 3 4