Октет
Cтраница 4
Бор заполняет свой октет также при образовании анионов типа BF7 и ВН7, [ НВ ( ОК) 3Г и [ В ( С Н5) 4Г и внутрикомплексных соединений типа 10.1. Было доказано, что четыре связи бора в таких хелатах приблизительно тетраэдрические ( и, что совершенно определенно, не плоские), поскольку в случае лигандов. [46]
Но не всегда октет может быть образован таким образом. Это имеет силу только для ряда газообразных веществ, элементы которых образуют друг с другом молекулы. Электроны октета расположены парами. Если электроны непарные, то они называются электронами связи. Они соединяются в электронные пары. Такой вид связи называют атомной связью. Число атомных связей соответствует атомной валентности элемента. Вещества, образованные благодаря атомной связи, имеют, как правило, низкие точки кипения и плавления. Они состоят из отдельных молекул. [47]
Благодаря этому образуются октеты для каждого атома. Двойные связи не фиксированы в определенных местах, а перемещаются, придавая каждой связи в известной мере характер двойной связи. [48]
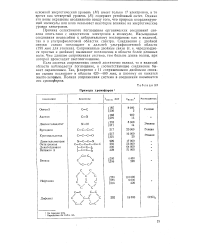 |
Примеры хромофоров. [49] |
N) содержит устойчивый октет. Однако эти ионы окрашены неодинаково ввиду того, что природа координирующей молекулы или иона оказывает некоторое влияние на энергетические уровни электронов. [50]
Хотя лангмюровским термином октет Льюис и сам пользуется, он полагает, что Лангмюр переоценил и абсолютизировал правило октета. Я думаю, - писал Льюис, - что энтузиазм Ланг-мюра, связанный с этой идеей, ввел его в заблуждение и что, называя новую теорию октетной теорией, он чересчур выпячивает то, что в конце концов представляет собой лишь одну черту новой теории валентности. Правило восьми, несмотря на его большую важность, менее фундаментально, чем правило двух [ там же, стр. [51]
Склонность к заполнению октета путем присоединения электронов и образованию отрицательных ионов, резко выраженная у элементов VII группы и в меньшей степени - у элементов VI группы, в данном случае еще менее характерна. Ионы N3 -, P3 - и As3 существуют только в твердом состоянии в некоторых нитридах, фосфидах и арсенидах металлов. Эти соединения легко гидролизуются, образуя гидриды соответствующих элементов и окиси металлов. Неустойчивость этих ионов объясняется тем, что они обладают слишком большим избытком отрицательных зарядов ( три электрона) по отношению к положительным зарядам ядер. Как уже было показано, мышьяк, сурьма и висмут проявляют все возрастающую склонность к образованию положительных ионов в растворе. [52]
Теория дублета - октета применима только в тех случаях, когда не рассматриваются атомы высших периодов ( S, Si, Р и др.) - Для этих атомов известны стабильные соединения с участием как 10, так и 12 электронов. [53]
В терминах правила октетов и электронных эффектов формула Полин-га, по-видимому, является наиболее удачным изображением особого ароматического состояния связей в молекуле бензола. [54]
Другой способ заполнения октета на атоме бора заключается в, обобществлении я-электронов, рассмотренном в гл. [55]
Страницы: 1 2 3 4