Оландер
Cтраница 1
Оландер 31 дал общий метод решения и несколько примеров в отношении влияния на скорость абсорбции обратимых реакций, скорость которых достаточно велика, чтобы обеспечивать равновесие во всех точках в пленке. Представляется возможным до некоторой степени обобщить его выводы. [1]
Оландер [80] показал, что при кратковременном контакте имеют место большие отклонения от модели Хандлоса и Барона. Причина этого в том, что при математических расчетах авторы использовали только один член ряда. Такой прием допустим для длительного, но не для кратковременного контакта. [2]
Оландер и Бенедикт [124] изучали кинетику экстракции воды в диффузионной ячейке с перемешиванием и нашли, что вода распределяется физически. В работе [75] отмечено поверхностное сопротивление, обусловленное образованием гидратов ТБФ. Недавно Хеффенден и Так [ 761 изучали молекулярную диффузию воды через границу раздела фаз вода - ТБФ. [3]
 |
Образование семикарбазона в условиях общего кислотного катализа. [4] |
Интересно, что Оландер [138] в 1927 г. пытался объяснить наличие колоколообразной зависимости скорости образования оксимов от рН изменением в стадии, определяющей скорость реакции. [5]
Уравнение (V.132), как указали Секор и Бойтлер 34, было опубликовано Оландером 31 с опечаткой. Здесь оно дано в исправленном виде. [6]
 |
Определение влаги ( в %, удерживаемой различными волокнами. [7] |
Необычные свойства при экстракции воды проявляет система трибутилфосфат-углеводород. Оландер и Бенедикт [220 ] пришли к выводу, что экстракция системой трибутилфосфат-н-гексан протекает как процесс массообмена. [8]
Оландер [169] отметил, что тогда как корреляция Вильке-Ченга обычно является удовлетворительной для многих растворенных органических веществ, диффундирующих в воде, то в противоположном случае диффузии воды в органическом растворителе пользоваться ею для определения коэффициентов диффузии нельзя. [9]
Бюри и Оландер [5], а также Тидман 6 ] в Скинингрове ( Англия) в 1919 - 1921 гг. сделали попытку получения спирта сернокислотным методом, также применяя в качестве сырья коксовый газ с содержанием около 2 % этилена. Было найдено, что концентрация кислоты должна составлять 95 - 95 8 %, а температура 60 - 80 С. [10]
В качестве одной из возможных причин возникновения СПБ часто указывают [9, 21, 22] на возникновение при массопередач флуктуации плотности, приводящих к отклонению движения жидкости от баротропности. Так, Оландер и Редди [13], изучавшие экстракцию HNO; в системе вода - растворы трибутилфосфата в н-гексане и ССЬ, приходят к выводу, что нестабильность плотности не может быть причиной возникновения СПК. В этой системе водная фаза-находится на; органической и при переходе HN03 из воды в органическую фаз5 плотность последней на поверхности раздела фаз была бы выше, чем в остальном объеме фазы. Так как органическая фаза расположена под поверхностью раздела, то коэффициент массопередачг из водной фазы в органическую увеличился бы, если бы причиной возникновения СПК являлась нестабильность плотности, что н согласуется с опытом. [11]
Более тщательное исследование диффузии воды в различных органических жидкостях было выполнено Лисомм и Саррамом [124], Некоторые данные, рассмотренные этими авторами, представлены в табл. 11.3, Выводы сделать трудно. В одних случаях предпочтительнее корреляция Вильке-Ченга, в других модификация, предложенная Оландером. Иногда обе методики неприменимы. [12]
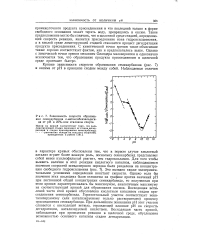 |
Зависимость скорости образования семикарбазона о-метоксибензальдеги-да от рН в 25 % - ном этиловом, спирте. [13] |
Такое предположение могло бы означать, что в щелочной среде стадией, определяющей скорость реакции, является присоединение иона гидроксиламмония, а в кислой среде лимитирующей стадией становится процесс дегидратации продукта присоединения. С кинетической точки зрения такое объяснение также хорошо соответствует фактам, как и предполагалось выше. Однако с химической точки зрения механизм Оландера маловероятен и однозначно исключается тем, что образование продукта присоединения в щелочной среде протекает быстро. [14]
В работе [60] исследована кинетика экстракции HNO3 смесями ТБФ с ССЦ. Равновесие при распределении кислоты характеризовалось приведенным ранее уравнением / С Сор / Свр ( Cs - Cop), поэтому интегральная форма уравнения массопередачи с постоянным общим аналитическим коэффициентом массопередачи более сложная, чем в случае уравнения Оландера. [15]
Страницы: 1 2