Биосинтез - порфирин
Cтраница 1
Биосинтез порфиринов у фотосинтезирую-щих бактерий осуществляется таким же способом, как и у других организмов. [1]
Второй пример-это биосинтез порфиринов, главным предшественником которых тоже является глицин. [3]
Для этой цели удобно биосинтез порфиринов разбить на ряд этапов. [4]
Различные отклонения от нормального течения биосинтеза порфиринов ведут к нарушениям ряда функций организма. Изменение механизма превращения порфобилиногена в уропорфирин является наследственным и приводит к возникновению очень редкого заболевания - врожденной порфирии. Основная масса порфиринов, образующихся в нормальном организме, относится к типу III; порфирины типа I образуются в очень небольшом количестве и легко выводятся из организма. При врожденной порфирии, однако, аутоконденсация порфобилиногена протекает так, что образуется уропорфириноген I, который не может быть далее использовав в биосинтезе тема и превращается в уро - и копропорфирины I. Эти порфирины не могут распадаться с образованием желчных пигментов и откладываются в организме ( кости и зубы больного пигментированы и флуоресцируют при облучении ультрафиолетовым светом) или экскретируются. Порфирины, циркулирующие в крови, вызывают фотосенсибилизацию кожи, результатом чего являются тяжелые ожоги, и фотосенсибилизиро-ванный гемолиз эритроцитов, который стимулирует усиленный синтез гемоглобина и, следовательно, порфиринов типа I, а это еще более отягощает состояние организма. [5]
На стадии протопорфирина происходит разветвление путей биосинтеза порфиринов в животных и растительных организмах. У растений в порфириновое ядро внедряется магний, и магниевый комплекс через ряд стадий превращается в хлорофилл. У животных образуется железо-протопорфириновый комплекс - гем. Внедрение железа катализируется ферментом феррохелатазой ( или гем-синтетазой), связанным с митохондриями. [6]
Итак, во всех описанных выше случаях присутствуют все или многие ферменты биосинтеза порфиринов, однако способность синтезировать АЛК, по-видимому, очень низка - обычно блокирован синтез АЛК. Содержание других ферментов биосинтеза порфиринов также может возрастать при изменении условий. [7]
Аминолевулиновая кислота ( АЛК) и пор-фобилиноген ( ПЕГ), несомненно, являются двумя первыми соединениями на пути биосинтеза порфиринов, причем ПБГ - это первое соединение данного пути, у которого все атомы углерода обычно уже необратимо связаны с биосинтезом порфиринов. [8]
При отравлении некоторыми веществами ( снотворными, сульфамидными препаратами, хиноном, производными свинца) или после ряда тяжелых болезней биосинтез порфиринов также нарушается, однако результатом этого является не порфирия, а пор-фиринурия - повышенная экскреция порфиринов с мочой. [9]
Аминолевулиновая кислота ( АЛК) и пор-фобилиноген ( ПЕГ), несомненно, являются двумя первыми соединениями на пути биосинтеза порфиринов, причем ПБГ - это первое соединение данного пути, у которого все атомы углерода обычно уже необратимо связаны с биосинтезом порфиринов. [10]
Итак, во всех описанных выше случаях присутствуют все или многие ферменты биосинтеза порфиринов, однако способность синтезировать АЛК, по-видимому, очень низка - обычно блокирован синтез АЛК. Содержание других ферментов биосинтеза порфиринов также может возрастать при изменении условий. [11]
Хлороз, сопровождающий этиолирование или недостаток железа, вполне мог бы быть обусловлен отсутствием или неактивностью какого-то одного фермента метаболизма порфиринов, например АЛК-синтетазы. Либо отсутствие одного или более специфических ферментов биосинтеза порфиринов могло бы просто отражать общий низкий уровень синтеза белка в клетке в целом или же в пластидах. Например, у кукурузы, страдающей от недостатка железа, фракция пластидных белков на 82 % меньше, чем обычно [101]; кроме того, свет, стимулирующий образование хлорофилла, активирует также образование некоторых белков, принимающих участие в фотосинтезе, например НАДФ-специфичной триозофосфатде-гидрогеназы в листьях проростков фасоли [83] и у эвглены [123], цитохрома / - типа у Суа-nidium caldarium [69] и у Euglena [142] и фико-билипротеидов у С. [12]
Продигиозин ( рис. 8.7) - один из нескольких вторичных бактериальных метаболитов, имеющих необычную структуру, в которой метоксибипиррольный фрагмент включен в дипиррометиленовую структуру. Известно, что биосинтез продигиозина не связан с биосинтезом порфирина. Таким образом, интересно было выяснить, каким путем происходит биосинтез продигиозина. Родственные системы были ранее исследованы при помощи радиоактивной 14С - метки. [13]
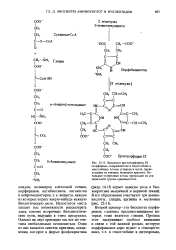
Опыты с глицином, меченным 14С, показали, что углерод метиленовой группы глицина внедряется в положения 4, 9, 14, 16 колец А, В, С и D порфинового ядра и образует, кроме того, все четыре метеновых мостика, но карбоксильная группа глицина не участвует в образовании пор-фирина. Остальные двадцать шесть углеродных атомов молекулы про-топорфирина образуются из метильной и карбоксильной групп уксусной кислоты; однако из распределения активности в молекуле протопорфи-рина видно, что уксусная кислота участвует в биосинтезе порфиринов в виде какой-то четырехуглеродной единицы. Как было показано, такой четырехуглеродной единицей является янтарная кислота, возникающая из ацети-кофермента А в цикле трикарбоновых кислот ( см. стр. Лимонная и а-кетоглутаровая кислоты, лежащие на пути превращения уксусной кислоты в янтарную в этом цикле, таким образом, также участвуют в биосинтезе порфиринов. [14]
Уже много лет назад было известно, что моча пациентов, страдающих порфирией, через несколько часов окрашивается в темно-красный цвет. Ответственное за окраску вещество было выделено Весталлом [32] и позднее идентифицировано как порфобилиноген ( ПБГ); в то время еще не было достаточно однозначно установлено, что порфобилиноген является промежуточным соединением в биосинтезе порфиринов. Позднее было показано, что ПБГ включается в гем с большей эффективностью, чем АЛК, и, следовательно, порфобилиноген представляет собой дополнительное звено в биосинтезе порфиринов. Для проявления максимальной каталитической активности фермента необходимо присутствие тиольных реагентов. Гетерологичные пирролы типа ( 25) образуются при инкубации фермента со смесью АЛК ( 1) и левулиновой кислоты ( 24); отсюда следует, что молекула субстрата, ковалентно связанная с ферментом по типу основания Шиффа, ответственна за формирование части молекулы ПБГ, несущей боковую карбоксиметнльную группу. [15]
Страницы: 1 2