Биосинтез - триптофан
Cтраница 1
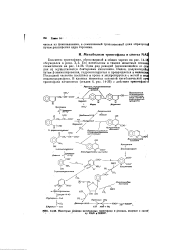 |
Некоторые реакции катаболизма триптофана и реакции, ведущие к син - ie. [1] |
Биосинтез триптофана, обрисованный в общих чертах на рис. 14 - 1J обсуждался в разд. Один ряд реакций ( начинающийся со ста дни а) осуществляется бактериями кишечника. Индол, получающийс путем В-элиминирования, гидроксилируется и превращается в индоксил Последний частично поступает в кровь и экскретируется с мочой в в индоксилсульфата. [2]
Биосинтез триптофана из индола и / - серина был осуществлен Татумом и Боннером [288] с помощью недостаточной по триптофану разновидности плесени Neurospora crassa Позднее Бутенандт [ 289 1 пришел к мысли о возможности химического синтеза / - триптофана на тех же общих основаниях, которые он использовал для конденсации индола с соединением, содержащим элементы аланиновой цепочки. [3]
Биосинтез триптофана из индола и / - серина был осуществлен Татумом и Боннером [288] с помощью недостаточной по триптофану разновидности плесени Neurospora crassa. [4]
Биосинтез триптофана начинается с образования антранилата, причем донором аминогруппы является КНг-группа глутамииа. На последней стадии, катализируемой ферментом триптофан синтазой, происходит перенос индолыюго гете-роцикла от глицерин фосфата на атом С при гпдрокснгрупне серпиа, сопровождающейся отщеплением гидрокспгруппы серииа в виде молекулы воды и превращением гидрокенгруппы остатка глпцерпнфосфата в альдегидную. [5]
При биосинтезе триптофана 5-фосфорибсзилпирофосфат взаимодействует с антраниловой кислотой. Образующийся рибозид С претерпевает перегруппировку Амадори ( см. стр. [6]
Значительно лучше у высших растений изучен вопрос биосинтеза триптофана из индола и серина. [7]
Этот оперон состоит из пяти генов, кодирующих ферменты биосинтеза триптофана. Регуляцию осуществляют две системы, чувствующие потребность клетки в триптофане. Первая система влияет на эффективность инициации на промоторе оперона. Репрессор триптофанового оперона в комплексе с триптофаном присоединяется к оператору, расположенному перед стартовой точкой транскрипции в районе - 10, и стерически препятствует РНК-полимеразе присоединяться к промотору. Таким образом, при избытке триптофана оперон репрессирован. В отсутствие триптофана репрессор теряет способность связываться с оператором, в результате чего оперон индуцируется. В условиях избытка триптофана лишь одна из десяти молекул РНК-полимеразы, начавших синтез РНК на триптофановом промоторе, преодолевает этот терминатор и переходит в область структурных генов. При уменьшении количества триптофана доля молекул РНК-полимеразы, преодолевающих аттенюатор, возрастает. [8]
Его ДНК включается в хромосому вблизи - генов, кодирующих ферменты, ответственные за биосинтез триптофана. [9]
Продукт первой из них, индол ( 39), служит субстратом во второй, но пока комплекс ар2 действует как одно целое, обнаружить индол как истинный промежуточный продукт в биосинтезе триптофана невозможно. [10]
Основные исследования по синтезу ИУК из L-триптофана были сделаны на высших растениях. Кроме того, на высших растениях были проверены этапы биосинтеза триптофана. Правда, эти данные пока еще не нашли своего окончательного подтверждения. [11]
Второе объяснение причин снижения содержания индолилуксусной кислоты при цинковой недостаточности выдвинуто Тсуи ( Tsui, 1948), который показал, что при недостатке цинка резко снижено содержание триптофана - предшественника индолилуксусной кислоты. Тсуи пришел к выводу, что роль цинка в биосинтезе ауксинов является косвенной и связана с его влиянием на биосинтез триптофана. Позже было установлено ( Nason, 1950; Tsui, 1960), что при недостатке цинка резко снижен синтез триптофана из индола и серина. [12]
Содержится в растениях и микроорганизмах. Кофермент - пиридоксальфосфат, связанный па 3-субъединице. Катализирует конечную р-цию биосинтеза триптофана: индол-3 - глнцерофосфат - f - L - ce - рии I. ТРИСАХАРИДЫ, олигосахариды, содержащие в молекуле 3 моносахаридных остатка. При кислотном гидролизе расщепляются до моносахаридов, избират. [13]
Глн, Gin), L - y - no - луамид - L глутаминовой к-ты, заменимая аминокислота. В составе белков и в свободном виде встречается в жидкостях и тканях всех живых организмов. Важнейшее соединение азотистого обмена, с помощью к-рого в организме переносятся аминогруппы. Участвует в биосинтезе триптофана ( антраниловой к-ты), гис-тидина, пуринов, гексозаминов, рибофлавина, фолиевой к-ты и др. Служит ( вместе с аспарагином) растворимым NHz-содержащим резервным соединением для синтеза белков у растений. [14]
Страницы: 1