Зависимость - диссоциация
Cтраница 1
 |
Зависимость степени диссоциации электролита от концентрации раствора. [1] |
Зависимость диссоциации от концентрации растворов одинакова для всех электролитов, причем при уменьшении концентрации степень диссоциации, как это видно из табл. 19, увеличивается. [2]
Зависимость диссоциации от концентрации растворов одинакова для всех электролитов, причем при уменьшении концентрации степень диссоциации, как это видно из табл. 9, увеличивается. [3]
Рассмотрим зависимость диссоциации от присутствия постороннего электролита. Здесь надо различать два случая: первый - когда один из ионов одинаков у обоих электролитов, и второй - когда одноименных ионов у них нет. В первом случае это влия - ние обычно бывает более сильным. [4]
Рассмотрим зависимость диссоциации от присутствия постороннего электролита. Здесь надо различать два случая: первый - когда один из ионов одинаков у обоих электролитов, и второй - когда одноименных ионов у них нет. В первом случае это влияние обычно бывает более сильным. [5]
Рассмотрим зависимость диссоциации от присутствия постороннего электролита. Здесь надо различать два случая: первый - когда один из ионов одинаков у обоих электролитов, и второй - копда одноименных ионов у них нет. В первом случае это влия-вие обычно бывает более сильным. [6]
На рис. 1 приведена зависимость диссоциации продуктов гидролиза тетрахлорида титана от температуры и времени нагревания. [7]
Так как у различных веществ зависимость диссоциации и ионизации от температур различна, то в общем случае нельзя энергетическое состояние газообразного тела характеризовать термодинамической температурой. [8]
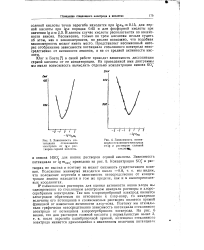 |
Зависимость потенциала стеклянного электрода от Ige растворов серной кислоты.| Зависимость потенциала стеклянного электрода OTlg а растворов соляной кислоте. [9] |
Юнг и Блетц [7] в своей работе приводят зависимость диссоциации серной кислоты от ее концентрации. [10]
Даже в пределах одного спектрального класса фикобилипротеиды различных видов могут отличаться друг от друга характером кривых, описывающих зависимость диссоциации и реаг-регации от рН, а также аминокислотным составом и иммунологическими свойствами. Однако сравнительные исследования в этой области весьма немногочисленны. [11]
Диссоциацию и тем самым силу кислоты обычно выражают константой диссоциации k, выведенной из закона разведения, покачивающего зависимость диссоциации слабой кислоты от се концентрации. Эта зависимость вытекает из следующих рассуждений. [12]
Диссоциацию и тем самым силу кислоты обычно выражают константой диссоциации k, выведенной из закона разведения, показывающего зависимость диссоциации слабой кислоты от ее концентрации. Эта зависимость вытекает из следующих рассуждений. [13]
Таким образом, диссоциация кислот подчиняется тем же закономерностям, что и диссоциация солей. Однако зависимость диссоциации кислот от свойств растворителя значительно сложнее. Важнейшую роль играет сродство растворителей к протону, а также способность растворителей образовывать продукты присоединения с молекулами кислот за счет водородных связей. [14]
Изучая электропроводность йодистого тетраэтиламмония в нескольких десятках растворителей, он нашел, что произведение электропроводности на вязкость при бесконечном разбавлении представляет постоянную величину. Вальдену принадлежит также обстоятельное изучение зависимости диссоциации электролитов от диэлектрической постоянной органических растворителей. [15]
Страницы: 1 2