Зависимость - константа - скорость - химическая реакция
Cтраница 1
Зависимость константы скорости химической реакции от температуры характеризуется также температурным коэффициентом скорости реакции К, или температурным градиентом скорости реакции At. Температурный коэффициент К, есть отношение констант скорости реакции при двух температурах, отличающихся на 10 С, т.е. это величина, показывающая, во сколько раз изменяется скорость реакции при изменении температуры на 10 С. Температурным градиентом скорости реакции At называют изменение температуры, необходимое для увеличения скорости реакции в 2 раза. [1]
Зависимость константы скорости химической реакции от температуры для гомогенных реакций характеризуют также температурным коэффициентом или температурным градиентом скорости реакции. [2]
Это выражение показывает зависимость константы скорости химической реакции от давления. [3]
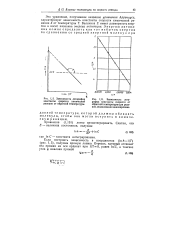 |
Зависимость логарифма константы скорости химической реакции от обратной температуры.| Зависимость логарифма константы скорости от обратной температуры для реакции дециклизации циклопропана. [4] |
Это уравнение, получившее название уравнения Аррениуса, характеризует зависимость константы скорости химической реакции k от температуры Т, Величина Е имеет размерность энергии и носит название энергии активации. [5]
А, АО, х является одновременно уравнением Аррениуса, выражающим зависимость константы скорости химической реакции от температуры, и уравнением, выражающим закон Бугера - Ламберта - Бера для поглощения света в веществе. [6]
Как показано в § 1 этой главы, число столкновений z, найденное на основании опытных данных по зависимости константы скорости химической реакции от температуры, в большинстве случаев не совпадает с рассчитанным из числа активных столкновений. [7]
Как показано в § 1 этой главы, число столкновений г, найденное на основании опытных данных по зависимости константы скорости химической реакции от температуры, в большинстве случаев не совпадает с рассчитанным из числа активных столкновений. [8]
Как уже было сказано в § 1 этой главы, число столкновений z, найденное на основании опытных данных по зависимости константы скорости химической реакции от температуры, в большинстве случаев не совпадает с рассчитанным из числа активных столкновений. [9]
Применение метода переходного состояния значительно расширило возможности теоретического подхода к решению кинетических задач. К числу результатов, которые могут быть получены при помощи этого метода ( без знания потенциальных поверхностей, определяющих течение элементарных актов), относится, в частности, зависимость константы скорости химической реакции от давления. [10]
Иногда удобнее, а часто и желательнее, обрабатывать экспериментальные данные в форме зависимостей, коэффициенты которых имеют определенный физический смысл. Удобство состоит в том, что некоторая зависимость может быть описана с достаточной точностью специальной функцией с меньшим числом параметров, а следовательно, с меньшими ошибками вычислений. С другой стороны, например, зависимость константы скорости химической реакции как функции температуры может быть аппроксимирована полиномом, однако целесообразнее ее описывать уравнением Аре-ниуса, когда параметрам этого уравнения придается конкретный физический смысл. [11]
Страницы: 1