Зависимость - равновесная концентрация
Cтраница 1
Зависимость равновесной концентрации Ср от температуры нелинейна. [1]
 |
Зависимость равновесного содержания метанола в газовой смеси от давления при разной температуре ( мольное соотношение Н2. СО в исходном газе 4. 1. [2] |
Зависимость равновесной концентрации метанола при разной температуре от давления представлена на рис. 10.1. С повышением температуры равновесная концентрация метанола значительно понижается, особенно резко при давлениях до 20 МПа. С повышением давления концентрация метанола растет. Следовательно, для достижения одной и той же концентрации метанола в реакционной смеси по мере повышения температуры требуется все более высокое давление. [3]
Зависимость равновесной концентрации NO от температуры при Р - 1 ата для различных соотношений воды в исходной смеси представлена на рис. 1.2. Равновесные кривые имеют перегиб с максимумом для азотно-водяной смеси при Г3600 К, а для воздушно-водяной смеси - при Г 3500 / С. Полученные кривые показывают, что с увеличением количества воды в исходной смеси равновесная концентрация оксидов азота снижается, причем для смесей воды с воздухом это снижение значительнее по сравнению со смесью воды с азотом. [4]
Зависимость равновесных концентраций фенолов в паре над кипящим щелочно-фенолятным раствором от степени связывания в нем едкого натра фенолами определялась экспериментально. Эксперименты проводились с водными растворами сме си фенолов, выделенных из производственных сточных вод и едкого натра. Эта кривая пригодна для области концентрации в растворе едкого натра 8 - 14 %, что соответствует обычно применяемым концентрациям на производственных установках. [5]
Если зависимость равновесных концентраций извлекаемого вещества в газовой фазе у от содержания его в абсорбенте х выражается в координатных осях х-у линией, близкой к прямой, то среднюю движущую силу можно определить, как среднюю арифметическую ( или среднюю логарифмическую при различии более, чем в два раза) движущих сил для низа и верха колонны. В общем случае среднюю движущую силу находят другими методами, описанными в специальной литературе, в частности графическим интегрированием. [6]
Рассмотрим зависимость равновесных концентраций продуктов сложных реакций от давления. [7]
В этом разделе зависимость равновесной концентрации м мера от степени полимеризации была выведена кинетическим методом. [8]
Важную роль играют зависимости равновесных концентраций компонентов в паре у ( Т) и в жидкости х ( Т) от температуры. [9]
В этом разделе зависимость равновесной Концентрации мономера от степени полимеризации была выведена кинетическим методом. [10]
Полагаем далее, что зависимость равновесной концентрации 1-го компонента 71 от Jj определяется формулой (6.35), а равновесная концентрация 2-го компонента постоянна. [11]
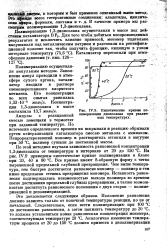 |
Кинетические кривые полимеризации диоксолана при различных температурах. [12] |
По этой методике изучали зависимость равновесной концентрации 1 3-диоксолана от температуры в интервале от 20 до 150 С. На рис. IV.9 приведены кинетические кривые полимеризации в блоке при 20, 40 и 80 С. Все кривые имеют S-образную форму с четко выраженной предельной глубиной превращения. Чем выше температура, тем быстрее достигается равновесие мономер - полимер и тем ниже предельная степень превращения мономера. [13]
Полагаем далее, что зависимость равновесной концентрации 1-го компонента AI от DI определяется формулой (5.176), а равновесная концентрация 2-го компонента постоянна. [14]
Полагаем далее, что зависимость равновесной концентрации 1-го компонента Л от t) i определяется формулой (5.176), а равновесная концентрация 2-го компонента постоянна. [15]
Страницы: 1 2 3 4 5