Описание - молекула
Cтраница 1
Описание молекулы в ТМО, в противоположность описанию ее в ТВС, дает возможность выяснить электронный спектр молекулы. Описание включает молекулярные ор-битали, не занятые электронами в невозбужденной молекуле. Эти орбитали позволяют судить о возможных переходах электрона при ее возбуждении. [1]
Описание молекулы с точки зрения ТМО позволяет оценить также полярность отдельных связей в ней ( стр. [2]
Описание молекулы по методу МО в предположении, что она содержит мостиковые метильные группы, показывает, что все связывающие орбитали заполнены. [3]
Описание молекул требует изложения теории химической связи, в которой важное место занимает явление расщепления уровней. Следует обратить внимание, что наличие дискретных уровней и пространственные особенности орбиталей ведут к образованию правильны, геометрических структур - четко выраженных, яапример, в молекулах комплексных соединений. [4]
Описание молекул с нелокализованными связями на основе метода молекулярных орбит не уступает проводимому на основе метода валентных связей. Для описания собственных функций электронов, охватывающих несколько атомов, используется нулевое приближение теории возмущения, подобно тому, как это выше сделано при рассмотрении иона молекулы водорода. Однако число слагаемых в функции будет равняться не двум, как это имело место в этой задаче, а будет равно числу атомов, которые охватывает общая молекулярная орбита. Так, л-электроны бензола охватывают шесть атомных орбит. [5]
Описание молекулы бензола сводилось к тому, что она состоит из атомов углерода и водорода, которые, в свою очередь, построены из электронов и ядер. При использовании концепции резонанса это описание дополняется следующими сведениями: структура молекулы бензола в основном состоянии соответствует резонансу между двумя структурами Кекуле с небольшим участием других валентных структур. [6]
 |
Расположение элементов в порядке их электроотрицательности. [7] |
Описание молекулы метана с точки зрения теории валентности представляет интерес в различных отношениях. [8]
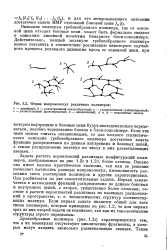 |
Форма макромолекул различных полимеров. [9] |
Описание молекулы гребнеобразного полимера, где от основной цепи отходят боковые цепи, может быть формально сведено к описанию линейной молекулы бинарного блок-сополимера. [10]
Более строгое кваитовомеханичеекое описание молекул будет дано в разд. [11]
Для описания молекул с нечетным числом электронов или молекул, свойства которых не соответствуют описанию классической ТВС, например для описания ароматических углеводородов, часто объединяют представления ТВС и ТМО. [12]
При описании молекулы в приближении Борна - Оппенгей-мера мы относим координаты электронов к ядерной системе отсчета. [13]
При описании указанных молекул язык ТМО легко переводится на язык ТВС, если за единицу химической связи принять два избыточных связывающих электрона. Так, например, на языке ТМО связь в ряду молекул Н2, F2, C2, N2, BN описывается соответственно двумя ( Н2, F2), четырьмя ( С2) и шестью ( N2, BN) избыточными связывающими электронами, а на языке ТВС связь в этих же молекулах описывается соответственно одной, двумя и тремя единицами связи. [14]
При описании молекулы водорода по теории молекулярных орбит мы должны поступать аналогично тому, как мы строили функции атомов при обсуждении периодической системы. Будем, как и всегда, одевать электронами голые, локализованные в определенных местах пространства ядра, занимая поочередно различные состояния, учитывая их энергии и выполняя запрет Паули. [15]
Страницы: 1 2 3 4